Espectroscopia optica
- 1. ESPECTROSCOPÍA ÓPTICA (Espectroscopia UV-Visible) CRISTHIAN Y. HILASACA ZEA
- 2. Una de las labores más difíciles dentro de la Química Orgánica es la elucidación estructural. En algunos casos es suficiente con algunos datos mínimos. Utilizando algunas propiedades Fisico-Químicas (punto de fusión, punto de ebullición, respuesta frente a los oxidantes, comportamiento frente a soluciones reveladoras…etc) y comparando estos datos con la bibliografía, podemos determinar la estructura de algunos compuestos. Es posible también conocer la fórmula molecular mediante un análisis elemental. Todas estas técnicas son aplicables a compuestos conocidos y descritos en la bibliografía. Nuestra labor se complica si hemos de analizar compuestos novedosos o de estructura muy compleja. Esta labor es casi diaria en un laboratorio de Química Orgánicaeta, en estos casos necesitamos métodos de análisis muy precisos y que utilizan pequeñas cantidades de compuesto para la determinación. INTRODUCCIÓN
- 4. 1. Introducción Métodos Instrumentales de Análisis: – Métodos ópticos. Clasificación – Radiación electromagnética – Espectro electromagnético 2. Absorción de radiación electromagnética 3. Fundamentos de la espectrofotometría de absorción UV-Vis – Teoría de la absorción de radiación UV-Vis – Espectro de absorción – Especies absorbentes. Tipos de transiciones electrónicas – Bases del color 4. Leyes de la absorción de la radiación: Ley de Lambert – Beer – Limitaciones y Desviaciones de la Ley de Beer 5. Instrumentación 6. Aplicaciones analíticas – Características analíticas del método – Análisis cuantitativo. Detalles del procedimiento experimental – Aplicaciones al análisis de alimentos CONTENIDOS
- 5. 1. Introducción Están basados en la medida de propiedades químicas y físicas de los analitos con fines cualitativos y cuantitativos. La medida se realiza en un instrumento apropiado. Propiedad medida Método Instrumental Método Instrumental Absorción de radiación Espectrofotometría de absorción Óptico Emisión de radiación Espectroscopía de emisión Óptico Potencial eléctrico Potenciometría Electroanalítico Corriente eléctrica Voltamperometría Electroanalítico Resistencia eléctrica Conductimetría Electroanalítico Métodos Instrumentales de Análisis
- 6. Métodos que miden alguna propiedad de la radiación electromagnética emitida por la materia o que interacciona con ella Clasificación Métodos espectroscópicos: Existe intercambio de energía entre la radiación electromagnética y la materia •Métodos de absorción: Miden la disminución de la potencia de la radiación electromagnética debida a la absorción que se produce en su interacción con el analito •Métodos de emisión: Miden la radiación electromagnética emitida cuando el analito es excitado por energía térmica, eléctrica o radiante Métodos no espectroscópicos: Se producen cambios en la dirección o en las propiedades físicas de la radiación electromagnética: Dispersión Refracción Difracción Rotación óptica Métodos ópticos de análisis 1. Introducción
- 7. • La radiación electromagnética es una forma de energía que se transmite por el espacio a gran velocidad sin soporte de materia. • La radiación electromagnética puede describirse según: la teoría ondulatoria: formada por ondas sinusoidales la teoría corpuscular: flujo de partículas o corpúsculos de energía llamados fotones La radiación electromagnética 1. Introducción
- 8. 1. Introducción • La radiación electromagnética (REM) se representa como ondas consistentes en campos eléctricos y magnéticos que están en fase y que oscilan sinusoidalmente de manera perpendicular entre sí y respecto a la dirección de propagación Dirección x Campo eléctrico y Campo magnético z Teoría ondulatoria . Parámetros ondulatorios Longitud de onda λ Amplitud A •La potencia P: es la energía del haz que llega a un área dada por segundo Parámetros ondulatorios
- 9. La radiación electromagnética es considerada como paquetes discretos de energía llamados fotones o cuantos. Dualidad onda-partícula: Un fotón es una partícula de radiación electromagnética con masa cero y energía E proporcional a la frecuencia de la radiación ϑ La energía de un fotón: E = h ϑ •E = energía del cuanto de radiación: Cal mol-1 •ϑ = frecuencia de la radiación : hertzio (Hz) = ciclos s-1 •h = constante de Planck = 6,624 • 10-27 erg s Velocidad de la luz : v = ϑ λ Velocidad de la luz en el vacío: c = 3,00 • 1010 cm s-1 Energía de un fotón :E = h ϑ = h c /λ Cuando λ aumenta, disminuye la energía y frecuencia del fotón Teoría corpuscular. Propiedades corpusculares de la radiación electromagnética λ µm = 10-6 m nm = 10-9 m Å = 10-10 m 1. Introducción
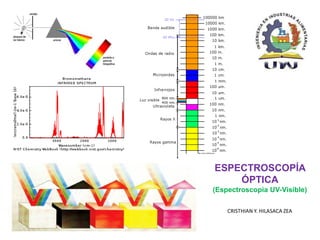
- 10. • Abarca un intervalo muy amplio de longitudes de onda o energías. • Según su λ recibe diferentes nombres. • La luz visible, que es la única perceptible por el ojo humano, representa solamente una pequeña parte del espectro, desde 350-380 a 750-780 nm. Espectro electromagnético 1. Introducción
- 11. 2. Absorción de radiación electromagnética Absorción: proceso por el cual una especie, en un medio transparente, capta selectivamente ciertas frecuencias de la radiación electromagnética. El fotón absorbido hace pasar a la especie de su estado fundamental a un estado excitado de energía M*: M + h ϑ → M* Tras un corto período de tiempo, aproximadamente 10-8 a 10-9 s, se pierde la energía de excitación, generalmente en forma de calor, y la especie M vuelve a su estado fundamental: M* → M + calor Los métodos de absorción tienen la ventaja de producir poca o ninguna alteración en el sistema estudiado.
- 12. Para que la radiación electromagnética sea absorbida por la materia deben cumplirse dos condiciones generales: 1) debe haber una interacción entre el campo eléctrico de la radiación y alguna carga eléctrica de la sustancia 2) La energía de la radiación incidente debe ser exactamente igual a la energía cuantizada que requiere la sustancia. Ecuación de Bohr ΔE = Ef – Ei = h ϑ h ϑ: energía del fotón absorbido Ei: energía total de la materia en el estado fundamental Ef: energía total de un estado permitido de energía superior o estado excitado. Requisitos 2. Absorción de radiación electromagnética
- 13. 3. Fundamento de la Espectrofotometría de Absorción UV-visible Método instrumental óptico basado en la medida directa de la absorción de radiación electromagnética UV-Visible, por las moléculas del analito contenido en la muestra. • La región ultravioleta comprende entre 10 y 400 nm y la región visible comprende entre 350 y 750 nm. • Las radiaciones UV y visible tienen en común el hecho de que la absorción de ambas regiones por moléculas, provoca la excitación de e- de enlace a niveles de E superiores. • Los picos de absorción pueden correlacionarse con los tipos de enlaces de la especie absorbente, base de su aplicación cualitativa
- 14. Un analito molecular tiene la capacidad de absorber ciertas longitudes de onda características de la radiación electromagnética UV-Visible. En este proceso, la radiación es transferida temporalmente a la molécula y, como consecuencia, disminuye la intensidad de la radiación. Dicha disminución, debida a la absorción experimentada por el analito, puede ser cuantificada utilizando diversas magnitudes, siendo la Absorbancia, A, la más comúnmente utilizada en la espectrofotometría de UV-Vis. La aplicación cuantitativa de la espectroscopía de absorción UV-Vis se basa en la medida, a una λ fija, de la A de una disolución del analito contenida en una cubeta transparente de camino óptico b cm. 3. Fundamento de la Espectrofotometría de Absorción UV-visible
- 15. E0 E1 E2 ΔE1 = E1-E0=hδ1 = hc/λ1 ΔE2 = E2-E1=hδ2= hc/λ2 Espectro de absorción Cubeta Radiación incidente P0 b Radiación transmitida P Disolución de analito de concentración c Transmitancia = T = P/P0 Absorbancia = A = - log T = log P0 /P Atenuación de un haz de radiación por una especie absorbente contenida en la cubeta Transiciones energéticas en la molécula del analito Absorbancia A λ, nm 3. Fundamento de la Espectrofotometría de Absorción UV-visible
- 16. Transmitancia: fracción de radiación que una sustancia deja pasar cuando la REM atraviesa la muestra. Transmitancia = T = P/P0 T puede valer desde 0 hasta 1. %T puede valer desde 0 hasta 100 % Absorbancia: es la atenuación de la intensidad de la radiación cuando ésta incide sobre una muestra. Es la cantidad de energía que la sustancia toma para pasar a un estado más excitado. A aumenta a medida que aumenta la atenuación de la radiación. Cuando no hay absorción de radiación Po= P y entonces A = 0,, mientras que si se absorbe el 99% de la radiación, solo se transmite el 1%, la A = 2 Transmitancia y absorbancia Absorbancia = - log T = log P0 /P 3. Fundamento de la Espectrofotometría de Absorción UV-visible
- 17. Un espectro de absorción es una representación gráfica de la absorbancia de un analito (o de otra magnitud equivalente) en función de la longitud de onda de la radiación λ (o de otro parámetro relacionado con la energía de la radiación utilizada). El máximo de absorbancia obtenido en el espectro de absorción de un analito, nos dará la longitud de onda que proporciona la mayor sensibilidad posible, y por tanto será la que se utilizará en el análisis espectrofotométrico de dicho analito. Espectros de absorción Absorbancia A λ nm λmax 3. Fundamento de la Espectrofotometría de Absorción UV-visible
- 18. La sensación de color se produce cuando disminuye apreciablemente una o más zonas de la región visible. •Si el ojo recibe luz de todas las λ de la región visible el efecto es luz blanca. •El color aparente siempre es el color complementario del que ha sido eliminado. •Los colores complementarios son útiles para predecir la λ de absorción de los compuestos coloreados: una disolución amarilla, absorberá luz azul 450-480 nm, para analizarla debemos usar luz con esta λ seleccionada con el monocromador o bien usar un filtro azul, que transmite esta luz azul Teoría del color 3. Fundamento de la Espectrofotometría de Absorción UV-visible
- 19. amarillo-verde 520 - 550 violeta 380 - 420 amarillo 550 - 580 420 - 440 anaranjado 580 - 620 azul 440 - 470 rojo 620 - 680 verde-azul 470 - 500 púrpura 680 - 780 verde 500 - 520 verde 500 - 520 púrpura 680 - 780 verde-azul 470 - 500 rojo 620 - 680 azul 440 - 470 anaranjado 580 - 620 azul-violeta 420 - 440 amarillo 550 - 580 violeta 380-420 amarillo-verde 520 - 550 Color absorbido λ (nm) complementario Color observado λ (nm) Una disolución se observa de color azul cuando se ilumina con luz policromática, porque absorbe λ 580-620 nm (anaranjado) y transmite o deja pasar λ 440-470 nm (azul) azul-violeta 3. Fundamento de la Espectrofotometría de Absorción UV-visible
- 20. • Para cada estado electrónico en una molécula existen varios estados vibracionales y para cada uno de éstos, numerosos niveles rotacionales. • Etotal= Eelectrónica + Evibracional + Erotacional • La radiación absorbida por la molécula puede ser utilizada para originar las diversas transiciones electrónicas posibles. • ΔE = Ef – Ei = h ϑ = Energía del fotón absorbido Diagrama de niveles de energía Teoría de la absorción molecular. Cambios de energía durante la absorción E 3 2 1 0 3 2 1 0 3 2 1 0 E0 E1 E2 VIS UV Absorción molecular λ1 λ4 λ´1 λ´4 3. Fundamento de la Espectrofotometría de Absorción UV-visible
- 21. Especies absorbentes Las especies absorbentes: moléculas orgánicas y aniones inorgánicos que tienen electrones: • en orbitales moleculares σ • en orbitales moleculares π • en orbitales no enlazantes n. Tipos de transiciones electrónicas : Cuando absorben fotones de E adecuada se pueden dar 4 tipos de transiciones electrónicas: • σ → σ * • n→ σ * • π → π* • n→ π* Transiciones electrónicas entre niveles de energía moleculares n * * 3. Fundamento de la Espectrofotometría de Absorción UV-visible
- 22. Especie absorbente Sus electrones más exteriores o electrones de enlace pueden ser elevados a niveles de E más altos al incidir sobre ellas una radiación electromagnética apropiada Grupo cromóforo • Grupo atómico presente en una molécula que lleva asociada una banda de absorción electromagnética: C=C; C=O; C=N. • Especies con grupos funcionales con enlaces π. • Grupos cromóforos →dobles y triples enlaces. • Bandas en el UV cercano y visible. • Etileno, carbonilo, éster, amida, nitro… Grupo auxocromo Grupos que no producen por sí mismos bandas de absorción, pero intensifican la de los grupos cromóforos: C-Br; C-OH Responsables del color de muchos iones y compuestos de metales de transición que poseen orbitales d y f Bandas de campo ligando 3. Fundamento de la Espectrofotometría de Absorción UV-visible
- 23. 4. Leyes de la absorción de la radiación Al interaccionar la radiación electromagnética con la materia, tiene lugar la absorción si la ϑ de la radiación coincide con la energía necesaria para que el sistema pase a un nivel de energía superior y permitido h ϑ = E2 - E1 Las dos leyes fundamentales que rigen el comportamiento de la fracción de la radiación incidente absorbida al pasar a través de una muestra dada son: Ley de Lambert: predice el efecto que produce el espesor del medio-muestra sobre la fracción de radiación que se absorbe. Ley de Beer: establece el efecto de la concentración del medio-muestra sobre la fracción de radiación que se absorbe. Ley de Lambert-Beer
- 24. Ley de Lambert-Beer: muestra cómo la absorbancia es directamente proporcional a la longitud b de la trayectoria a través de la solución y a la concentración c del analito o especie absorbente. c b a A · · c b A · · a: cte de proporcionalidad llamada absortividad. (unidades L/cm·g, si c=g/L) b: longitud del camino que recorre la radiación a través del medio absorbente. c: concentración expresada en g/L (mg/L, ...). Si la concentración c viene expresada en mol/L, la cte de proporcionalidad se denomina absortividad molar y se representa por (unidades L/cm·mol). La absortividad molar, , es característica de cada especie a una λ determinada -Disoluciones que contienen varias especies absorbentes: Para cada λ: Atotal =∑Ai = A1 + A2 + .... + An Como A = · b · c A = 1 · b · c1 + 2 · b · c2 + …. +n · b · cn Siendo 1, 2, …, n los componentes absorbentes. 4. Leyes de la absorción de la radiación
- 25. Ley de Lambert- Beer AT,l = log P0 P = b c Absorbancia total medida a la longitud de onda l Concentración molar de las especies absorbentes camino óptico Potencia del haz después de atravesar la muestra Potencia del haz antes de atravesar la muestra P P0 = Transmitancia (T) A = -logT Absortividad molar A = b c Ley de Lambert- Beer 4. Leyes de la absorción de la radiación
- 26. • La Ley de Beer debe comprobarse siempre antes de utilizarla para un análisis cuantitativo exacto. • Para ello se preparan una serie de disoluciones estándar del analito en el intervalo en el que se supone que se encuentra la muestra. • Se registra el espectro de absorción utilizando una de ellas. • Se mide la absorbancia de dada una de las disoluciones a la λ del máximo de absorción del analito con una longitud de cubeta dada, generalmente 1 cm. • Se representan las absorbancias en función de las concentraciones. • Si la ley de Beer se cumple en todo el intervalo de c estudiado: A = εbc se obtiene una línea recta en todo el intervalo, que pasa por el origen. • La recta obtenida se llama Curva de calibrado. • Pueden aparecer desviaciones positivas o negativas a partir de una determinada concentración debido a Limitaciones de la ley de Beer y/ó a posibles errores experimentales cometidos Comprobación de la Ley de Beer. Curva de calibrado 4. Leyes de la absorción de la radiación
- 27. Desviaciones de la Ley de Beer La proporcionalidad directa entre absorbancia y concentración cuando b es constante, sólo se cumple en un intervalo de concentraciones del analito. Fuera de dicho intervalo se observan en las curvas de calibrado desviaciones positivas o negativas de la linealidad debido a las limitaciones de la Ley de Beer: A concentración Para la aplicación cuantitativa, las medidas de A de la muestra deben estar incluidas en el intervalo lineal respuesta debida a la autoabsorción o a la luz escasa que atraviesa la cubeta respuesta del blanco, interferencias o escasa sensibilidad A= εbc Intervalo lineal 4. Leyes de la absorción de la radiación
- 28. • Limitaciones propias o reales – Variación de la absortividad con el índice de refracción n, que varía con la c. – Para c < 0,01 M n= cte: Ley de Beer se cumple. • Incumplimiento de las premisas de la ley de Beer. – Interacciones entre el soluto y la radiación producidas por mecanismos distintos al de absorción. – Interacciones entre las especies absorbentes del soluto . – Radiación no monocromática. Limitaciones de la Ley de Beer 4. Leyes de la absorción de la radiación
- 29. • Errores químicos. – Efectos debidos a sistemas en equilibrio: • equilibrios de dimerización • equilibrios ácido-base • equilibrios de complejación – Efectos debidos al disolvente. – Efectos debidos a impurezas absorbentes de los reactivos. – Efectos debidos a la presencia de interferencias absorbentes en la muestra. • Errores instrumentales. – Errores de lectura: • El mínimo error relativo se obtiene para una absorbancia de 0,434 • Las absorbancias deben estar comprendidas entre 0,2 y 0,8 para obtener el mínimo error – Radiación parásita. • Errores personales: – Utilización y cuidado de las cubetas de absorción. – Control de Temperatura. Errores al aplicar la Ley de Beer 4. Leyes de la absorción de la radiación
- 30. 5. Instrumentación Componentes básicos de los espectrofotómetros Fuente de energía radiante Selector de λ Detector Dispositivo de lectura Cubeta muestra Luz compuesta Monocromador I0 I b Luz monocromática Fuente de radiación Detector Muestra
- 31. 300 500 700 900 Lámpara de Deuterio Lámpara de Tungsteno o Wolframio longitud de onda (nm) intensidad lumínica 1100 Fuente de energía radiante Continua. Estable. Intensa Para λ en el Visible Para λ en el Ultravioleta Características 5. Instrumentación
- 32. Selector de λ Filtros de corte Filtros de absorción Filtros de interferencia •longitud de onda de máxima transmisión •ancho de banda efectivo Características Monocromadores de prisma Monocromadores de red Fotómetros Espectrofotómetros 5. Instrumentación
- 33. Cubetas Absorción mínima a la longitud de onda de trabajo Colocar con caras transparentes perpendiculares a la dirección del haz incidente Características Vidrio o plástico Visible Sílice Ultravioleta 5. Instrumentación
- 34. Detectores •deben responder a un amplio rango de longitudes de onda •deben dar respuesta rápida •deben ser sensibles a bajos niveles de radiación •deben producir señal eléctrica fácilmente amplificable •la señal debe ser proporcional a la potencia radiante Su función es convertir la respuesta del instrumento en una señal medible. Características Fototubos Fotomultiplicadores Fotodiodoarray 5. Instrumentación
- 35. Espectrofotómetros Haz sencillo Doble haz Fuente de radiación Sistema selector de λ Cubeta de muestra Fotodetector Registrador o PC Fotocelda 1 Fotocelda 2 Cubeta de referencia Amplificador Fuente de radiación Sistema selector de λ Amplificador diferencial Registrador o PC Cubeta de muestra Cubeta de referencia 5. Instrumentación
- 36. La espectrofotometría de absorción molecular se puede aplicar tanto al análisis cualititativo como cuantitativo. Análisis cualitativo: los espectros de la muestra se comparan con los de los correspondientes estándares, con el fin de identificar las bandas de absorción coincidentes. Este tipo de análisis es más frecuente en UV e IR para identificar compuestos orgánicos y más rara vez se utiliza en Vis. Análisis cuantitativo: está basado en la ley de Lambert-Beer en el intervalo de concentraciones de cumplimiento de la ley. •Se establece la curva de calibrado usando estándares y la absorbancia de la muestra de concentración desconocida se remite a la curva (a veces basta con un solo estándar). •En espectrofotometría Vis, el analito se suele incorporar a una especie compleja que presente bandas de absorción intensas. •Siempre que sea posible se debe medir la absorbancia a λmax 6. Aplicaciones analíticas
- 37. Amplia aplicabilidad: Análisis orgánico e inorgánico Elevada sensibilidad: los límites detección de 10-4 a 10-5 M. Selectividad de moderada a alta. Buena exactitud: errores de concentración 1-5% o incluso menores. Facilidad y comodidad en las medidas espectrofotométricas. Se prestan a una fácil automatización. Campo de aplicación Especies absorbentes: compuestos orgánicos que contengan grupos cromóforos y especies inorgánicas como son los metales de transición. Especies no absorbentes: los analitos reaccionan con un reactivo para producir un compuesto absorbente. Características de los métodos espectrofotométricos 6. Aplicaciones analíticas
- 38. Toma y tratamiento de la muestra Selección de la longitud de onda Control de las variables que influyen en la absorbancia Determinación de la relación entre la absorbancia A y la concentración c Metodología cuantitativa. Detalles del procedimiento experimental •Realizar un espectro de absorción de la muestra •Para obtener máxima sensibilidad, realizar las medidas de A a una λ que corresponda a un máximo de absorción λmax, ya que el cambio en la absorbancia por unidad de concentración es mayor en este punto. •la naturaleza del disolvente •el pH de la disolución •la temperatura •las concentraciones altas del electrolito •la presencia de sustancias interferentes Elegir las condiciones para el análisis •Calibración con patrones de concentración conocida •Método de las adiciones estándar a) El método de un solo punto b) El método de las adiciones múltiples 6. Aplicaciones analíticas
- 39. Pocas veces es posible suponer el cumplimiento de la ley de Beer y utilizar un único patrón para determinar la absortividad molar. Comprobar la ley de Beer realizando un calibrado a la λ del máximo de absorción. Se miden las absorbancias de patrones y muestras y se obtiene la ecuación de la recta de calibrado generalmente aplicando el método de mínimos cuadrados: A = mc + b Los estándares o patrones de calibración se deben aproximar tanto como sea posible a la composición final de las muestras reales y deben abarcar un intervalo razonable de concentraciones del analito. La concentración de la muestra se calcula a partir de la ecuación de la recta de calibrado sustituyendo su valor de A y despejando la c correspondiente Calibración con patrones de concentración conocida Metodología cuantitativa. Detalles del procedimiento experimental 6. Aplicaciones analíticas
- 40. Calibración con patrones de concentración conocida Analito en la muestra A muestra A (l = 508 nm ) 6. Aplicaciones analíticas
- 41. Cuando se analizan muestras complejas, como alimentos ó cenizas vegetales, suele ser imposible o muy difícil preparar estándares que se asemejen a las muestras. En este caso, el método de las adiciones estándar es útil para contrarrestar los efectos de matriz. Método de las adiciones estándar Método de las adiciones estándar. El método de un solo punto •Se toman dos porciones de la muestra •Una porción se mide como de costumbre •A la segunda porción se le agrega una cantidad conocida de la disolución estándar de analito •Ambas respuestas se utilizan entonces para calcular la concentración desconocida, suponiendo una relación lineal entre la respuesta y la concentración del analito Metodología cuantitativa. Detalles del procedimiento experimental 6. Aplicaciones analíticas
- 42. •Absorbancia de la primera disolución A1 = K cx cx concentración desconocida de analito en la 1ª disolución K constante de proporcionalidad. •Absorbancia de la segunda disolución A2 = (K vx cx / v t) +( K v s c s / v t) vx volumen de la disolución de concentración desconocida de analito, vs volumen agregado de la disolución estándar de analito, v t es el volumen total después de la adición y cs es la concentración de la disolución estándar de analito cx = A1 v s cs / A 2 v t - A1 vx Método de las adiciones estándar. El método de un solo punto 6. Aplicaciones analíticas
- 43. Método de las adiciones estándar. El método de las adiciones múltiples •Varias alícuotas idénticas Vx de la solución desconocida con concentración Cx se transfieren a matraces volumétricos de volumen Vt. • A cada uno de esos matraces se le añade un volumen variable Vs de una disolución patrón del analito, con concentración conocida Cs. •Después, se añaden los reactivos que originan el color y se diluye cada solución hasta un volumen Vt. •Si el sistema químico sigue la ley de Beer, A i= (ε b Vs Cs / Vt ) + (ε b Vx Cx / Vt ) = K Vs Cs + K Vx Cx K es una constante = ε b / Vt •Una gráfica de AI en función de Vs debe originar una recta de la forma A i = m Vs + b Donde la pendiente m y la ordenada en el origen b vienen dadas por m = K Cs y n = K Vx Cx •El análisis de mínimos cuadrados de los datos se puede utilizar para determinar m y b; después, es posible calcular Cx a partir del cociente de esas dos cantidades y los valores conocidos de Vx y Cs Cx = (Cs / Vx ) ( n/m) 6. Aplicaciones analíticas
- 44. A = mc+b 0 = mc muestra + b Cmuestra = b/m Método de las adiciones estándar . El método de las adiciones múltiples Concentración añadida del estándar Concentración de la muestra A0 A1 A2 A3 c1 c2 c3 6. Aplicaciones analíticas
- 45. • La espectroscopia en la región ultravioleta-visible (UV-Vis) es una de las técnicas de laboratorio más comúnmente encontradas en el análisis de los alimentos. • Ejemplos: • Cuantificación de macrocomponentes (el contenido total de hidratos de carbono, por medio del método del fenol-ácido sulfúrico) • Las estimaciones de enranciamiento (el estado de la oxidación de los lípidos, por medio del ensayo del ácido tiobarbitúrico) • Determinación de pigmentos basada en su absorción de radiación en la zona del visible • Análisis del contenido de proteínas solubles. • Determinación de nitritos en jamón de York • Determinación de hierro en vinos • Determinación de fosfato en bebidas Aplicaciones al análisis de alimentos Especies que no absorben en el Visible: mediante su reacción previa con reactivos adecuados para dar un compuesto coloreado 6. Aplicaciones analíticas
