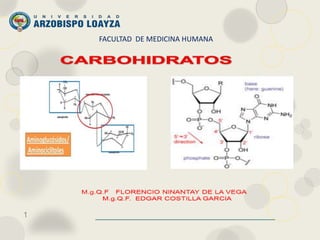
Carbohidratos - Bioquímica
- 1. 1 FACULTAD DE MEDICINA HUMANA
- 2. . 3
- 3. 4
- 4. OBTENCIÓN DE CARBOHIDRATOS Los carbohidratos son sintetizados por todos los vegetales verdes, a través del proceso denominado fotosíntesis, que se representa como sigue: 6CO2 + 6H2O + Luz → C6H12O6 + 6O2 (673 Kcal.) Tanto en el hombre como en los animales terrestres, los carbohidratos suministrados en la dieta son la principal fuente de energía metabólica (ATP). Esta reacción se representa de la siguiente manera: C6H12O6 + 6O2 → 6CO2 + 6H2O + 38 ATP
- 5. El término genérico "Carbohidrato" incluye monosacáridos, oligosacáridos derivadas de y polisacáridos, así como sustancias del grupomonosacáridos por reducción carbonilo (alditoles), mediante oxidación de uno o más grupos terminales a ácidos carboxílicos, o por la sustitución de un grupo hidroxi o más (s) por un átomo de hidrógeno, un grupo similares. "Azúcar" amino, un grupo tiol o grupos heteroatómicos También incluye derivados de estos compuestos. El término se aplica con frecuencia a los monosacáridos y oligosacáridos inferiores. Cabe señalar que aproximadamente el 3% de los (escompuestos enumerados por Chemical Abstracts Service decir, más de 360 000) son nombrados por los métodos de la nomenclatura de carbohidratos.
- 7. Son polihidroxialdehídos o polihidroxicetonas quirales o conducen compuestos que por hidrólisis a éstos.
- 8. NOMENCLATURA R-S CLASIFICACIÓN y NOMENCLATURA
- 9. ENANTIÓMEROS D y L Configuración del penúltimo átomo de carbono en relación con la del último . D-gliceraldehído L-gliceraldehído (Isomeros: 2n) OHH C HO C H CHO CHO CH2OH CH2O H D (+) L (-)
- 12. Epímeros Los azúcares que sólo difieren en la estereoquímica de un carbono se denominan epímeros y el átomo de carbono cuya configuración es opuesta generalmente se especifica. Si16no e especificael número de carbonos, se asume que es un C2.
- 15. 21 lumifeve@gmail.com Anómeros de LOS MONOSACÁRIDOS El carbono hemiacetal se denomina carbono anomérico, que se identifica con facilidad como el único átomo de carbono unido a dos oxígenos. http://www.stolaf.edu/people/giannini/flashanimat/carbohy drates/glucose.swf En el anómero α, el grupo hidroxilo del carbono anomérico (hemiacetal) está hacia abajo (axial) y en el anómero β hacia arriba (ecuatorial). El anómero β de la glucosa tiene todos sus sustituyentes en posiciones ecuatoriales.
- 16. REPRESENTACIÓN CONVENCIONAL DE LOS MONOSACÁRIDOS Fischer modificado Fischer Haworth de Arabinofuranose - L - representaciones - D - Ribopiranose
- 17. Mutarrotación Una solución acuosa de D-glucosa contiene una mezcla en equilibrio de α- D-glucopiranosa, β-D-glucopiranosa, y el un intermedio de cadena abierta. La cristalización por debajo de 98°C de 98°C da el anómero beta. da anómero alfa y la cristalización por encima
- 18. Son azúcares en los que se ha sido eliminado el oxígeno de un grupo hidroxilo. Entre los desoxiazúcares tenemos 2-desoxirribosa es uno de los componentes fundamentales del ADN. 2-D-desoxirribosa 6-desoxi-L-galactosa L-fucosa 6-desoxi-L-manosa L-ramnosa 2,6-Didesoxi-D-alosa Digitoxosa H O C CH2 H C OH H C OH H C OH CH3
- 19. Desoxiazúcares C En glicósidos naturales –antibióticos- Importancia de los ácidos desoxiribonucleicos DNA - L-ramnopiranosa 2-desoxi-D-ribosa 6-desoxi-- L-manopiranosa H O H C H H C OH H C OH CH2OH CH3 OH O OH OH HO
- 20. AMINOAZÚCARES 2-amino - 2-desoxi--D-glucopiranosa -D-glucosamina - 2-desoxi--D-galactopiranosa2-amino condroitina de -D-galactosamina Hidrólisis de la cartílagos y moco nasal OH CH2OH O HO NH2 OH Hidrólisis de la quitina de esqueletos de crustáceos e insectos HO CH2OH O HO NH2 OH
- 21. El ácido N-acetilmurámico, participa en la formación de su rigidez. derivado de la N-acetil-glucosamina, las paredes bacterianas y asegura así N-acetilmurámico N-neuramínico Ácido N-acetilneuramínico
- 22. Obtención de polioles CH2OH Sorbitol Manitol Ribitol D-glucosa D-manosa D-ribosa Humectantes Espesantes Goma de mascar xilitol Intermedarios Diuréticos H2/Pt Hexano EdulcorantesD-glucosa H2/Ni Catódica HO CH2OH OH HO HO HO CH2OH OH HO HO O
- 23. Obtención de ácidos aldónicos D-glucosa D-manosa D-arabinosa Ácido Ácido Ácido D-glucónico D-manónico D-Arabónico Acidificantes Espesantes Dosificación (Ca) Estabilizantes Br2/ H2O HO CH2OH OH HO HO COOH HO CH2OH OH HO HO O
- 24. Obtención de ácidos aldáricos COOH -D-manosa Ácido D-manárico HOO OH Doble--lactona del ácido D-manárico DesintosicantesComplejantesAcidificantes OH HO O O O O HO O O OH HNO3/ H2O HO OH OH HO COOH HO CH2OH OH O HO OH
- 25. Obtención de ácidos urónicos 2 2 HO -D-manosido Glicósido del ácido D-manurónico También lactonas de ácido urónico DesintoxicantesAcidificantes Complejantes Oxidación H O HO COOH OH O OR HO CH2OH OH O HO OR
- 26. GLICÓSIDOS O CH3 ENLACE GLICOSÍDICO ENLACE ACETAL ENLACE HEMIACETAL HO CH2OH O HO HO HO CH2OH O HO HO OH
- 27. Aglicones El grupo enlazado al carbono anomérico de un glicósido se denomina aglicón.
- 28. β mportantes son los disacáridos.Los más i En los disacáridos existe unión glicosídica, entre dos monosacáridos. En ellos es importante saber: cómo se verifica esta unión, a dónde, en qué posición está situado el enlace. Una unión muy común es la 1-4´, quiere decir, están comprometidos en el enlace, el C1, carbono anomérico de una unidad y el C4 de la otra unidad . O OOO Enlace 1-4´ β O O 4´ OH 1 OH
- 29. DISACÁRIDOS MALTOSA: Es el azúcar de malta. Grano germinado de cebada que se utiliza en la elaboración de la cerveza. Se obtiene por hidrólisis de almidón y glucógeno. Posee 2 moléculas de glucosa unidos por enlace tipo (1-4) 4-O-(α-D-glucopiranosil)-D-glucopiranosa CH2OH O HO HO OH CH2OH Hidroxilo hemiacetálico libre O O HO OHOH α-D-glucopiranosil (1→ 4) D-glucopiranosa 6-O-(α-D-glucopiranosil)-α-D-glucopiranosa
- 30. DISACÁRIDOS CELOBIOSA: No se encuentra libre en la naturaleza. Se obtiene por hidrólisis de la celulosa. y está formado por dos moléculas de glucosa unidas por enlace (1-4). O CH2OH Hidroxilo HO O OHOH 4-O-(β-D-glucopiranosil)-D-glucopiranosa β-D-glucopiranosil (1 →6) D-glucopiranosa CH2OH HO O hemiacetálico OH HO libre
- 31. DISACÁRIDOS LACTOSA: Es el azúcar de la leche de los mamíferos. Se encuentra formada por la unión (1-4) de la -D- galactopiranosa y la -D-glucopiranosa. 2 O CH OH Hidroxilo hemiacetálico HO O OHOH 4-O-(β-D-galactopiranosil)-D-glucopiranosa β-D-galactopiranosil (1→4) D-glucopiranosa OH CH OH 2 O OH HO libre
- 32. DISACÁRIDOS SACAROSA: Es el disacárido no reductor, ya que los dos carbonos anoméricos de la glucosa y -1,fructosa están implicados en el enlace G( -2). CH2OH4 HO 5 13 OH OCH2OH 1 α-D-glucopiranosil-β- D- fructofuranósido 6 O HO 2 6 O 5 OH 2 4 3 CH2OH OH
- 33. '.. ..' ...,-
- 34. Son polímeros naturales, llamados poliósidos o glucanos, macromoléculas, formadas por de de cientos o miles Dos de unidades monosacáridos. ejemplos típicos polisacáridos son el almidón y la celulosa. ALMIDÓN El almidón está formado por una cadena 14, con enlaces 16 en los puntos de ramificación. Los almidón dos son constituyentes principales del la amilosa y la amilopectina.
- 35. 62 lumifeve@gmail.com AMILOSA constituye de un 15 a un 20% del almidón y tiene estructura helicoidal no ramificada, soluble en agua, da color azul con el yodo.
- 36. Amilosa helicoidal. La amilosa helicoidal forma un complejo de transferencia de carga de color azul con el yodo molecular.
- 37. % del almidón y lumifeve@gmail.com ALMIDÓN AMILOPECTINA constituye un 80-85 consiste en residuos de cadenas muy ramificadas, de 24 o 30 lasglucosa unidos por enlaces 14 en cadenas y por enlaces 16 en los puntos de ramificación, insoluble en agua, da color rojo a púrpura con el yodo.
- 38. Polisacárido más abundante en la naturaleza, es el tejido de sostén de las plantas, está asociada con las hemicelulas y la lignina. La celulosa está formada por unidades de D(+)- glucosa, los enlaces en el polisacáridos son β 1,4´: de enlace los carnívoros no pueden romperlo y por pueden utilizar la glucosa como nutriente. La celulosa forma microfibrillas de 14 000 unidades o este tipo tanto no más, que se torcionan y se unen a otras por puente de hidrógeno. La masa molecular varía entre 250 000 y 1 x 106 o más. OHO CH2O H HO OH OHO O CH2O H OOH CH OH CH2OH O O O HO OH O HO O 2
- 39. l polisacárido que se almacena en lumifeve@gmail.com
- 40. or 67 lumifeve@gmail.com Polisacárido de gran Se importancia estructural en los losinvertebrados. puede encontrar en exoesqueletos de crustáceos e insectos. Las unidades básicas son N-acetil- -D-glucosaminas unidas p enlaces [14] glucosídicos.
- 42. cosaminoglucano, regula la hidratación e 69 lumifeve@gmail.com
- 43. lumifeve@gmail.com Es un glucosaminoglucanos, que son importantes extracelularconstituyentes estructurales de la matriz formandel cartílago, como los que los tejidos vasosconectivos del cuerpo, cartílago, piel, sanguíneos, así como los ligamentos y los tendones. -D-glucuronato(13)-4-sulfato-2-N-acetil- glucosamina -D-
- 44. ÁCIDOS NUCLEICOS
- 45. Polímero ARN Los ácidos nucleicos están formados por unidades de ribofuranósido enlazadas mediante uniones fosfato.
- 46. Enlaces fosfato Dos nucleótidos están enlazados mediante una unión fosfato entre el grupo fosfato 5' de uno y el grupo hidroxilo 3' de otro. Una molécula de ARN siempre tiene dos extremos (a no ser que esté en la forma de un gran anillo). Un extremo tiene un grupo 3' libre y el otro extremo tiene libre un grupo 5'.
- 47. Ribonucleótidos comunes. Son ribonucleósidos esterificados por el ácido fosfórico en su posición 5'; el grupo -CH2OH se encuentra en el extremo de la cadena de ribosa. Los ribonucleósidos se unen a través de enlaces de fosfato
- 48. Desoxirribonucleósidos comunes. Los cuatro desoxirribonucleósidos que constituyen el ADN La estructura del polímero de ADN es similar a la del ARN, excepto en que no tiene grupos hidroxilo en los átomos de carbono 2' de los anillos de ribosa.
- 49. NUCLEÓTIDOS Los nucleótidos, además de su papel en la formación de los ácidos nucleícos, tienen una función independiente y vital para la vida celular. Cuando un nucleótido se modifica por la unión de dos grupos fosfato, se convierte en un transportador de energía, necesario para que se produzcan numerosas reacciones químicas celulares. La energía en los nucleótidos modificados, esta disponible en cantidades convenientes y aceptado en forma generalizada. El principal portador de energía, en casi todos los procesos biológicos, es una molécula llamada adenosín trifosfato o ATP .
- 51. El éxito en la vida siempre adelante. consiste en seguir Samuel Johnson