Espectroscopia
- 1. A N À L I S I E S P E C T R O S C Ò P I C Interacció entre les radiacions electromagnètiques i la matèria
- 2. Energia de les radiacions electromagnètiques Una ona electromagnètica consisteix en un conjunt de paquets d’energia (quantums) , anomenats fotons Atès que els fotons són absorbits i emesos pels atòms, actuen com a transportadors d’energia L’energia d’un fotó () és directament proporcional a la freqüència de la ona (f) Equació de Planck: = h · f h = 6,626 ·10-34 J· s (constant de Planck)
- 3. Energia de les radiacions electromagnètiques Els efectes de cada tipus de radiació electromagnètica sobre els àtoms i molècules depèn de la energia de la radiació (de la seva i de la seva f)
- 4. Efectes de les radiacions sobre la matèria Efectes de les radiacions electromagnètiques sobre àtoms i molècules
- 5. Efectes de les radiacions sobre la matèria
- 6. Efectes de les radiacions sobre la matèria -Radiació γ : radiacions ionitzants produïdes en processos radioactius -Raigs X: fotoionització (arrenquen electrons d’àtoms i molècules) - UV: fotoionització (UV llunyà) i canvis de nivell energètic dels electrons (UV proper) - Visible: canvis de nivell energètic dels electrons - IR: moviments de vibració molecular - Microones: moviments de rotació i torsió de les molècules - Ones de ràdio: transicions d’espín nuclear en els àtoms (ressonància magnètica nuclear si s’aplica simultàniament un camp magnètic) Els àtoms i les molècules tenen els seus nivells d’energia quantitzats. Cada regió de l’espectre electromagnètic té fotons de l’energia requerida per provocar determinats tipus de processos:
- 7. Efectes de les radiacions sobre la matèria Aquestes interaccions entre radiació i energies de les molècules són les que s’aprofiten per l’anàlisi estructural dels compostos, ja que són característiques de cada molècula concreta. Així, l’espectroscòpia és una tècnica analítica experimental, molt usada en química i en física. Es basa en detectar l’absorció o emissió de radiació electromagnètica de certes energies, i relacionar aquestes energies amb els nivells d’energia implicats en transicions quàntiques de la substància a detectar. D’aquesta manera, es poden fer anàlisis quantitatius o qualitatius d’una enorme varietat de substàncies, aprofitant la capacitat d’emetre o absorbir la radiació d’una determinada longitud d’ona que presenten aquestes, o algun producte format a partir d’elles.
- 8. Mètodes espectroscòpics Per analitzar les substàncies actualment s’utilitzen diverses tècniques instrumentals basades en l’espectroscòpia : - Espectroscòpia d’espectre infraroig (IR): detecció de grups funcionals orgànics. - Espectrometria UV-visible : detecció d’enllaços múltiples, anàlisi quantitatiu. - Ressonància magnètica nuclear (RMN): determinació del tipus i posició dels àtoms d’hidrogen en les molècules orgàniques; obtenció d’imatges pel diagnòstic en medicina. - Espectrometria de masses (MS): determinació de la massa molecular i de l’estructura de les molècules. Per realitzar l’elucidació estructural de molècules normalment s’utilitzen les dades obtingudes a partir de diverses tècniques.
- 9. Espectroscopia infrarroja L'espectroscòpia infraroja és la branca de l'espectroscòpia que treballa amb la part infraroja de l'espectre electromagnètic Es basa en fer interaccionar una molècula amb radiació electromagnètica de la zona de l’infraroig, per a determinar quines radiacions concretes és capaç d’absorbir. Amb aquesta tècnica s’obté un espectre d’infraroig on es representa l’absorbància (o transmitància) per a cada radiació infraroja, mesurada habitualment pel seu nombre d’ona (o a vegades per la seva longitud d’ona o freqüència). Nombre d’ona (wavenumber) És la inversa de la longitud d’ona i per tant és proporcional a la freqüència. S’expressa en cm-1. 1 n
- 10. Espectroscopia infrarroja L'espectroscòpia infraroja és la branca de l'espectroscòpia que treballa amb la part infraroja de l'espectre electromagnètic Quan una molècula absorbeix radiació infraroja es produeixen canvis d’energia vibracional degut a les deformacions dels enllaços per tensió i flexió. L’energia d’aquest tipus de radiació és capaç de provocar un salt des del nivell fonamental d’energia vibracional a un nivell excitat. estirament simètric scissoring wagging estirament asimètric rocking twisting
- 11. Espectroscopia infrarroja L'espectroscòpia infraroja és la branca de l'espectroscòpia que treballa amb la part infraroja de l'espectre electromagnètic Els enllaços covalents vibren en determinades freqüències que es troben dins dels valors de les de l'espectre IR. Aquestes freqüències depenen de cada enllaç: Enllaç mínim nombre d’ona (cm-1) nombre d’ona màxima (cm-1) grup funcional C – O 1000 1300 Alcohols i èsters N – H 1580 1650 Amina o amida C = C 1610 1680 Alquens C = O 1650 1760 Aldehids, cetones, àcids, èsters, amides O – H 2500 3300 Àcids carboxílics (banda molt ampla) C – H 2850 3000 Alcans C – H 3050 3150 Alquens O – H 3230 3550 H enllaçat en els alcohols N – H 3300 3500 Amina o amida O – H 3580 3670 OH lliure en alcohols (només en les mostres diluïdes amb solvent no polar)
- 12. Espectroscopia infrarroja L'espectroscòpia infraroja és la branca de l'espectroscòpia que treballa amb la part infraroja de l'espectre electromagnètic Normalment s’estudia l’absorció IR de les substàncies en la regió del IR mitjà (200 – 4000 cm-1) Es fa incidir un raig de llum infraroja sobre una mostra d'una substància molecular i s'enregistra l'energia que absorbeix la substància en cada longitud d'ona. S'obté un gràfic en el qual es veu en quines λ la mostra ha absorbit energia.
- 13. Espectroscopia infrarroja Cada tipus d’enllaç absorbeix unes longituds d’ona característiques i això permet identificar els grups funcionals que té la molècula stretching vibrations: estiraments, tensions bending vibrations: flexions i torsions
- 14. Espectroscopia infrarroja Transmitància: Mesura de la capacitat d’una substància per a transmetre la radiació electromagnètica, expressada com la relació entre el flux de radiació transmesa i el flux de radiació incident.
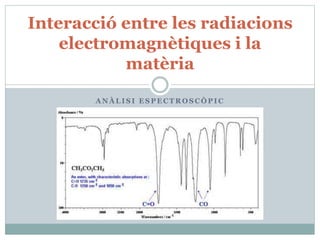
- 15. Argumenteu quin dels següents compostos, X, Y o Z, és compatible amb la fórmula i l’espectre infraroig donat: X: 3-pentanona CH3CH2COCH2CH3 Y: àcid pentanoic CH3CH2CH2CH2COOH Z: 2-penten-1-ol CH3CH2CH=CHCH2OH
- 16. ~ 2900 cm-1 C-H carboni enllaçat a un altre carboni amb enllaç simple, C-C) ~ 1710 cm-1 C=O És l'espectre IR de la 3-pentanona
- 17. Un exemple d’un problema resolt Com a subproducte en una síntesi s’ha obtingut una substància que, una vegada purificada i fet l’anàlisi elemental, dona una fórmula C4H8O i un espectre IR com el següent: De quin compost es pot tractar, de la butanona, del propanal o del 3-buten-1-ol?
- 18. Amb la mateixa fórmula molecular C4H8O tenim dos dels tres compostos isòmers pels que demana el problema: CH3-CO-CH2-CH3 CH2=CH-CH2-CH2-OH Ja que el propanal té per fórmula C3H6O i no por ser. L’espectre IR té un marcat pic a 1050 cm-1, un altre a 1650 cm-1 i una banda a 3200- 3500 cm-1, que podríem correspondre als enllaços C-O dels alcohols, a C=C dels alquens i al O-H dels alcohols, respectivament, i no s’aprecia un pic significatiu entre 1650-1760 cm-1 corresponent a l’enllaç C=O de les cetones. Podem concloure que estem davant el 3-buten-1-ol. C-O dels alcohols C=C dels alquens O-H dels alcohols
- 19. Ressonància magnètica nuclear (RMN) La RMN es basa en la interacció entre nuclis atòmics sota la influència d’un camp magnètic extern i un camp electromagnètic d’una freqüència determinada (ones de ràdio). La RMN s’utilitza rutinàriament en tècniques avançades d’obtenció d’imatges mèdiques, com en la Imatge per Ressonància Magnètica, i també com a eina espectroscòpica per obtenir dades físiques i químiques de compostos químics. Així com els espectres d’infraroig subministren informació sobre la presència o absència de grups funcionals en les substàncies que s’analitzen, els espectres de RMN de protó (també hi és la RMN d’altres elements, especialment la de carboni, que nosaltres no estudiarem) ens informaran del nombre, la naturalesa i l’ambient que envolta als hidrògens d’una molècula.
- 20. La RMN està relacionada amb el nucli dels àtoms. Ressonància magnètica nuclear (RMN) Els nuclis es comporten com a petits imants que, en situar-se en camps magnètics externs, es poden orientar a favor (paral·lels) o en contra (antiparal·lels) al camp magnètic. Els nuclis orientats en paral·lel tenen una energia inferior als situats en antiparal·lel. Hi ha una mica més del 50% dels nuclis orientats en paral·lel. Si s'aplica una radiació electromagnètica de radiofreqüència a una mostra, alguns dels nuclis absorbeixen energia i passen de la posició de paral·lel a antiparal·lel.
- 21. Ressonància magnètica nuclear (RMN) L'energia i, per tant, la freqüència de la radiació necessària depèn de la intensitat del camp magnètic on es troben els nuclis. Aquest valor depèn del camp extern i dels camps locals deguts als electrons dels àtoms veïns i dels grups que formen la molècula, que hi contribueixen amb petits camps magnètics. En el cas de l’espectroscòpia de RMN d’hidrogen l’energia necessària, és a dir, la freqüència, per a aconseguir el canvi d’orientació de l’espin nuclear es troba en la zona de radiofreqüència de l’espectre electromagnètic (300-600 MHz) i els camps magnètics aplicats en valors entre 7 i 14 T (Tesla)
- 22. Ressonància magnètica nuclear (RMN) Un espectròmetre de RMN consta d'un imant que produeix un camp magnètic fort, un emissor de radiofreqüències, un detector i un enregistrador. La mostra es posa entre els pols de l'imant, es manté el camp magnètic constant i s'hi aplica un pols electromagnètic dins de les radiofreqüències. En aplicar el pols de radiofreqüència hi haurà protons de la mostra que passaran de l'estat de baixa energia (paral·lel) al d'alta energia (antiparal·lel). Quan alguns d'aquests protons retornin al nivell inferior d'energia emetran radiació de la freqüència que correspon a la diferència d'energia, ΔE. La radiació emesa és la que es detecta i dóna lloc a l'espectre. La radiació és feble i el procés s'ha de repetir molts cops en una successió ràpida per tal de produir un registre acurat
- 23. La RMN està relacionada amb el nucli dels àtoms. Ressonància magnètica nuclear (RMN)
- 24. Depenent de l'entorn molecular on es troba el protó, el camp magnètic a què estarà sotmès serà lleugerament diferent. Els protons amb diferents entorns necessitaran diferent energia per passar de la posició de paral·lel a antiparal·lel, i per tant, absorbiran diferents freqüències de radiació. Com a resultat, apareixeran diferents pics RMN a l'espectre, que ens permetran diferenciar els diferents tipus d'hidrogen que hi ha a cada molècula, així com el seu nombre. Ressonància magnètica nuclear (RMN)
- 25. El senyal de TMS no interfereix i apareix a l’extrem de l’espectre de major camp. Ressonància magnètica nuclear (RMN) Les posicions de ressonància dels hidrògens es mesuren per comparació amb la posició dels protons d’una substància de referència, normalment els 12 hidrògens equivalents del tetrametilsilà (TMS, (CH3)4Si). Els seus 12 protons ressonen donant un senyal únic i nítid a camps més alts que qualsevol altre compost orgànic, ja que el silici és més electropositiu que els àtoms dels compostos orgànics. δ(desplaçament químic)
- 26. Ressonància magnètica nuclear (RMN) El desplaçament químic és adimensional i es dóna en parts per milió (ppm). Al pic del TMS se li assigna un valor de δ=0,000 ppm, i es defineix una escala fins a δ=12 ppm. D’aquesta manera el desplaçament químic d’un protó determinat és sempre el mateix en les mateixes condicions (dissolvent, temperatura, etc.), i no depèn de la freqüència de l’aparell utilitzat en la mesura. Intervals aproximats de desplaçaments químics de 1H situats en distints ambients químics.
- 27. L'àrea de cada pic és proporcional al nombre de protons de cada tipus. En l'espectre apareix un pic corresponent al tetrametilsilà (TMS), que s'ha escollit com a referència. La distància a la qual se situa un pic respecte al del TMS s'anomena desplaçament químic
- 28. Espectre de RMN d'un líquid incolor de fórmula molecular C2H6O. Quina és l'estructura del líquid? Possibles isòmers de fórmula molecular?
- 30. 2. L'espectre de RMN del metoxietà, CH3OCH2CH3, quants pics creus que tindrà? Quina proporció tindran les àrees dels pics? Resposta. Els 12 H del tetrametilsilà tenen el mateix entorn, mentre que en el metanol per una banda hi haurà els 3 H del grup metil i per l'altra el H de l'hidroxil. 1. Perquè creus que l'espectre de RMN del tetrametilsilà (TMS) amb dotze hidrògens té només un pic mentre que el metanol en té dos? L'espectre de RMN del metoxietà tindrà 3 pics, amb una proporció 3:2:3.
- 32. Espectrometria de masses (MS) Es vaporitza la mostra i es bombardeja amb un feix d'electrons d'alta energia (70eV). Les molècules de la mostra perden electrons externs i s'ionitzen. En el bombardeig també es pot produir fragmentació de les molècules, per trencament d'enllaços covalents i es formen fragments de la molècula amb càrrega positiva. Els ions produïts són accelerats en passar entre dues plaques carregades elèctricament. El feix d'ions carregats es fa passar a través d'un camp magnètic que provoca que els ions es desviïn. Els ions més lleugers es desvien més que els més pesants. Els ions desviats finalment impacten en el detector. Es processa i s'obté l'espectre de masses. Tot el sistema es troba sotmès a alt buit (l0-2 a l0-3Pa.) per a evitar col·lisions entre els fragments iònics generats.
- 33. Ió molecular (M+): ió més pesant que correspon a la molècula de pentà. Pic base: ió més abundant, el que dóna el senyal més fort i s'ajusta al valor del 100% de l'espectre. En aquest cas, correspon al fragment (M- 29)+ a CH3CH2CH2+.
- 38. Exemple d'exercici (PAU): Quan s’analitza la butanona, CH3CH2COCH3, per espectrometria de masses, s’obtenen els següents valors del quocient massa/càrrega: 72, 57, 43, 42, 29, 27 i 15. a) Indiqueu, breument, els processos bàsics que tenen lloc quan un compost és analitzat per espectrometria de masses. b) Indiqueu a quin ió poden correspondre els pics amb els valors de massa/càrrega 72 i 43, suposant que la càrrega és la unitat. Aquests dos pics es veurien si en lloc de la butanona s’hagués analitzat la propanona? Raoneu les respostes. Dades: Masses atòmiques relatives: C = 12; O= 16; H=1
- 40. a)Processos bàsics que tenen lloc quan un compost és analitzat per MS: −La mostra s’ha de volatilitzar i portar a pressions molt baixes. −El compost (M) es trenca en diferents fragments que tenen càrrega, normalment positiva i de valor unitat. Pot quedar compost sense trencar-se i carregat positivament (M+, ió molecular). −Els ions són accelerats en presència d’un camp elèctric. −Els diferents fragments carregats són separats segons el valor de la relació massa/càrrega que tenen. −Es detecta la quantitat de cadascun dels diferents fragments. b)Interpretació m/z 72 i 43, suposant que la càrrega és la unitat: La massa molecular de la butanona és 72. L’ió de quocient massa/càrrega 72 pot correspondre a la butanona ionitzada: CH3CH2COCH3+ (iómolecular). El pic de quocient m/z 43 pot correspondre al fragment CH3CO+, ja que el seu pes (dos carbonis, tres hidrògens i un oxigen) és de 43. Si enlloc de la butanona tinguéssim la propanona, CH3COCH3, no es veuria el pic de 72, perquè la propanona té menys massa molecular. Sí que es podria veure el pic de 43, ja que la propanona també pot fragmentar-se i donar l’ió CH3CO+, igual que feia la butanona.