Leishmaniose: doença causada por parasita transmitido por flebotomíneos
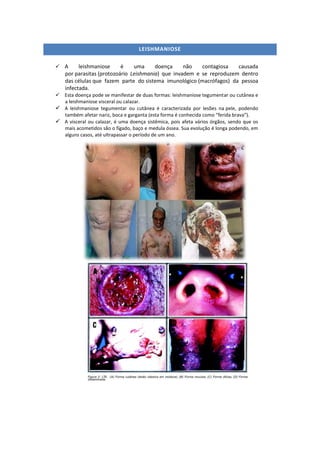
- 1. LEISHMANIOSE A leishmaniose é uma doença não contagiosa causada por parasitas (protozoário Leishmania) que invadem e se reproduzem dentro das células que fazem parte do sistema imunológico (macrófagos) da pessoa infectada. Esta doença pode se manifestar de duas formas: leishmaniose tegumentar ou cutânea e a leishmaniose visceral ou calazar. A leishmaniose tegumentar ou cutânea é caracterizada por lesões na pele, podendo também afetar nariz, boca e garganta (esta forma é conhecida como “ferida brava”). A visceral ou calazar, é uma doença sistêmica, pois afeta vários órgãos, sendo que os mais acometidos são o fígado, baço e medula óssea. Sua evolução é longa podendo, em alguns casos, até ultrapassar o período de um ano.
- 2. AGENTE VETOR: FLEBOTOMÍNEOS Os flebotomíneos são pequenos insetos responsáveis pela transmissão de algumas doenças aos humanos e animais, como a bartonelose, que é restrita aos altiplanos andinos, e várias arboviroses com ocorrência inclusive no Brasil. Porém, de maior importância, pela distribuição geográfica e número de casos, são as leishmanioses. Estes insetos pertencem à ordem Diptera, mesmo grupo das moscas, mosquitos, borrachudos e maruins. Apresentam um par de asas e um par de pequenas estruturas, chamados de halteres ou balancins, responsáveis pela estabilidade do vôo e zumbido característico dos dípteros. Os flebotomíneos apresentam um vôo curto. Na realidade eles saltitam na superfície de pouso e mantém as asas eretas, ou seja, levantadas para cima. No Brasil, são conhecidos por diferentes nomes de acordo com sua ocorrência geográfica, como tatuquira, mosquito palha, asa dura, asa branca, cangalhinha, birigui, anjinho, entre outros. Os flebotomíneos têm preferência por viver em locais com muita umidade e são vistos geralmente nas horas sem luminosidade e pouca movimentação de ar. Devido ao seu pequeno tamanho e sua fina cutícula, normalmente são encontrados em ambientes protegidos como fendas de pedra, buracos no solo, grutas de animais, ocos de árvore; e também em ambientes modificados pela ação humana, tais como: abrigos de animais domésticos (galinheiros, chiqueiros e currais). Sua atividade se dá em geral no crepúsculo noturno (final da tarde), mas em algumas situações específicas podem ocorrer durante as horas claras do dia, principalmente em locais associados à extensa cobertura florestal, como na Floresta Amazônica, ou restritas áreas da Mata Atlântica. PARASITA: LEISHMANIA As leishmania são protozoários parasitas de células fagocitárias de mamíferos, especialmente de macrófagos. São capazes de resistir à destruição após a fagocitose. As formas promastigotas (infecciosas) são alongadas e possuem um flagelo locomotor anterior, que utilizam nas fases extracelulares do seu ciclo de vida. O amastigota (intra-celular) não tem flagelo. Há cerca de 30 espécies patogênicas para o ser humano (CDC). As mais importantes são: o As espécies L. donovani, L. infantum infantum, e L. infantum chagasi que podem produzir a leishmaniose visceral, mas, em casos leves, apenas manifestações cutâneas. o As espécies L. major, L. tropica, L. aethiopica, L. mexicana, L. braziliensis, L. amazonensis e L. peruviana que produzem a leishmaniose cutânea ou a mais grave, mucocutânea.
- 3. TRANSMISSÃO Os machos de flebotomíneos se alimentam exclusivamente de alimentos açucarados, especialmente seiva das plantas; por outro lado, as fêmeas também realizam o repasto açucarado nas plantas ou na secreção de afídeos, que se constitui numa importante fonte de energia, porém, elas necessitam do sangue dos animais vertebrados para que ocorra a maturação dos seus ovos. Por essa razão, só elas são hematófagas, e conseqüentemente, estão envolvidas na transmissão de doenças aos humanos e animais. As fêmeas após realizarem o primeiro repasto sangüíneo em um reservatório natural do parasita (Leishmania), podem se infectar, ou seja, adquirir os protozoários. Estes irão sofrer processos de diferenciação e multiplicação no trato digestivo da fêmea. A digestão do sangue dura em torno de 72 horas em média, dependendo da espécie, porém após o sangue ser digerido e os ovos estarem amadurecidos, a grande maioria das fêmeas morrem após a postura dos ovos, já que há um desgaste energético extremo. As poucas fêmeas sobreviventes necessitam realizar uma segunda alimentação sangüínea, para da mesma forma maturarem seus ovos: é neste momento que elas transmitem a leishmaniose, pois no ato da picada injetam as formas flageladas (os protozoários) na corrente sangüínea de sua vítima. Vale ressaltar que a probabilidade de transmissão da doença vai depender das condições de exposição dos humanos aos flebotomíneos, assim como ao contexto eco- epidemiológico do ambiente. SINTOMATOLOGIA Os sintomas das leishmanioses variam de acordo com a espécie de protozoário. De modo geral, as tegumentares causam lesões na pele (mais freqüentemente ulcerações) e, em casos mais graves, atacam as mucosas do rosto, como nariz e lábios (leishmaniose mucosa). As leishmanioses viscerais causam febre, emagrecimento, anemia, aumento do fígado e do baço e imunodeficiência (diminuição da capacidade de defesa do organismo contra outros micróbios). Doenças causadas por bactérias (principalmente pneumonias) são a causa mais freqüente de morte nos casos de leishmaniose visceral, especialmente em crianças. PROFILAXIA Devido ao tamanho minúsculo, encontrar na natureza larvas e pupas de flebotomíneos é tarefa extremamente difícil, por essa razão não há nenhuma medida de controle que contemple as fases imaturas, ao contrário dos mosquitos que colocam seus ovos nos meios aquáticos, possibilitando seu controle através das formas não aladas. As medidas de proteção preconizadas consistem basicamente em diminuir o contato direto entre humanos e os flebotomíneos. Nessas situações as orientações são o uso de repelentes, evitar os horários e ambientes onde esses vetores possam freqüentar, a utilização de mosquiteiros de tela fina, dentro do possível, a colocação de telas de proteção nas janelas, evitar o acúmulo de lixo orgânico, mantendo sempre limpas as áreas próximas às residências e os abrigos de animais domésticos, fazer poda periódica nas árvores, para que não se criem os ambientes sombreados e realizar o manejo ambiental evitando o acúmulo do lixo orgânico, no sentido de afastados das casas os mamíferos comensais, como marsupiais e roedores, prováveis fontes de infecção para os flebotomíneos.
- 4. CICLO DE VIDA DO PARASITA O protozoário, em seu ciclo de desenvolvimento, assume duas formas evolutivas: amastigota (sem flagelo) e promastigota (flagelada). A primeira se desenvolve dentro do corpo dos hospedeiros e dos reservatórios. Uma vez lá, o amastigota multiplica-se no interior de células de defesa do sangue conhecidas como macrófagos. Quando o flebotomíneo se alimenta do sangue de um hospedeiro, infecta-se com os amastigotas que, então, se transformam em promastigotas. Na seqüência, os promastigotas reproduzem-se no tubo digestivo do inseto. Ao final de um processo de modificação, os promastigotas são inoculados em novos hospedeiros pela picada do flebotomíneo, nos quais voltam a assumir a forma de amastigotas, completando, assim, o ciclo evolutivo do parasito. A diversidade de espécies de Leishmania, associada à capacidade de resposta imune de cada indivíduo à infecção, está relacionada com as várias formas de manifestação da leishmaniose. As tegumentares são em geral menos graves, visto que seus efeitos restringem-se à pele e às mucosas. Já a leishmaniose visceral, como o próprio nome indica, afetam as vísceras (ou órgãos internos), sobretudo o fígado, o baço, os gânglios linfáticos e a medula óssea, podendo levar à morte quando não tratada. Até o momento, não se sabe bem por que algumas espécies de Leishmania (denominadas dermotrópicas) permanecem na pele e mucosas enquanto outras estão adaptadas ao parasitismo das vísceras. É possível que este fato esteja relacionado a diferentes graus de sensibilidade ao calor. TRATAMENTO Não há vacina contra as leishmanioses, assim como ainda não há para quaisquer doenças parasitárias humanas. Portanto, as medidas mais utilizadas para o combate da enfermidade se baseiam no controle de vetores e dos reservatórios. Para todas as formas de leishmaniose, o tratamento de primeira linha se faz por meio de remédios a base de antimoniais pentavalentes. Outras drogas, comumente utilizadas, são, como segunda escolha, a anfotericina B e a pentamidina.
- 5. EPIDEMIOLOGIA DAS LEISHMANIOSES TEGUMENTARES A incidência das leishmanioses tegumentares é cíclica, podendo haver um número alto de registros em um ano, baixo no outro e alto novamente no seguinte. Na última década, o registro de casos confirmados tem variado entre 30 mil e 40 mil por ano, no Brasil. Segundo dados da Secretaria de Vigilância em Saúde (SVS) do Ministério da Saúde, o maior coeficiente de detecção da doença se dá na Região Norte, onde ela atinge quase cem habitantes para cada cem mil. Em seguida, há as regiões Centro- Oeste, com 41,85, e Nordeste, com 26,50 casos para cada cem mil pessoas. Apesar dos números acima, a letalidade das leishmanioses tegumentares é inexpressiva, ocorrendo somente em casos esporádicos, como quando surgem infecções secundárias, ou quando ocorrem problemas na medicação do paciente. Muitos casos, inclusive, não são sequer registrados, ou porque o infectado não desenvolve a doença (tornando-se apenas um portador), ou porque o enfermo simplesmente não procura um serviço médico. Os ciclos no número de ocorrências explicam-se por fatores sociais e climáticos. Por exemplo, tais registros podem ser influenciados, de um lado, pelo desmatamento ou período de seca, por outro por algum processo de ocupação desordenada. Enfim, cada região apresentará características próprias, o que colabora para que os padrões de transmissão das leishmanioses tegumentares sejam de definição complexa. Ainda assim, tais padrões podem ser descritos em três linhas gerais: a transmissão florestal, a rural e a urbana. A transmissão florestal ocorre ao se penetrar nas matas. Por isso, ela atinge especialmente homens que se dedicam a profissões que exigem o contato silvestre, como a abertura de estradas, a coleta de produtos naturais, o garimpo, o turismo ecológico ou a extração de madeira. Os flebotomíneos envolvidos nesse primeiro padrão são essencialmente silvestres, assim como os animais que servem de reservatório para o agente causador (preguiças, tamanduás, gambás etc). Por isso, os casos por transmissão florestal concentram-se predominantemente na região Amazônica e no Centro-Oeste. O mosaico formado por pequenas porções florestais e áreas de baixa densidade demográfica servirá de ambiente perfeito para a transmissão rural. Neste caso, há espécies de flebotomíneos adaptadas tanto às matas quanto às áreas próximas aos domicílios. A infecção pode ocorrer em casa ou até mesmo quando uma criança vai para escola e passa por um pequeno bosque. Áreas rurais de ocupação antiga, sobretudo em estados como Ceará, Minas Gerais e Paraná, servem como exemplo. O padrão de transmissão urbana apresenta em dois aspectos: quando há o deslocamento do inseto transmissor das florestas para bairros próximos à mata, ou, simplesmente, pela ação de flebotomíneos adaptados a áreas arborizadas, periféricas à cidade. Um exemplo para o primeiro caso ocorre quando o perímetro urbano invade a floresta de modo desordenado. Ao ocorrer desmatamento nos limites urbanos para a construção de novas habitações, os animais silvestres das proximidades morrem ou fogem, o que deixa os flebotomíneos sem suas fontes alimentares naturais. Conseqüentemente, o inseto vai buscar nos animais domésticos e no homem o sangue necessário para a sua sobrevivência, levando consigo o protozoário. É o que acontece atualmente em Manaus, pois lá tem havido a devastação da floresta vizinha à cidade para a construção de novos bairros. No segundo caso, o vetor transmissor da doença já está adaptado ao espaço próximo aos domicílios. Angra dos Reis e diversas localidades de Paraty, ao sul do Estado do Rio de Janeiro, são exemplos clássicos, onde as transmissões urbanas são mais comuns. A presença das leishmanioses tegumentares, porém, em bairros completamente urbanos é praticamente impossível. No máximo, ela pode ocorrer em bairros periféricos com presença de matas alteradas, como em Jacarepaguá, na cidade do Rio de Janeiro. O combate à transmissão das leishmanioses tegumentares é difícil. O tratamento precoce dos casos ainda deve permanecer como prioridade do programa de controle desta endemia. Quanto às ações preventivas, é necessário haver uma adequação das
- 6. atividades de controle às condições de cada local atingido pela doença. As pesquisas e a política de enfrentamento contra a enfermidade devem ser adaptadas para cada região, não existindo uma fórmula geral. Contudo, uma coisa é certa: o alastramento do mal está intimamente ligado ao desequilíbrio ambiental, tema que deve ser sempre tratado como prioridade. EPIDEMIOLOGIA DAS LEISHMANIOSES VISCERAIS De acordo com o epidemiologista Paulo Sabroza, da Fiocruz, a atual situação da leishmaniose visceral no Brasil é grave. O quadro da doença só não é mais sério, em termos de risco potencial de epidemias em centros urbanos, que o do dengue. Até o início dos anos 80, a leishmaniose visceral restringia-se a bolsões de miséria, localizados majoritariamente no Nordeste. Hoje já é realidade em capitais como Teresina, São Luís, Campo Grande, Palmas e Belo Horizonte. Agora, aproxima-se de outras metrópoles como Brasília e São Paulo. "A questão não é se vai chegar, e sim quando vai chegar", alerta. Assim como nas tegumentares, a ocorrência da leishmaniose visceral é cíclica. De acordo com a SVS, mais de 70% dos casos ainda concentram-se no Nordeste. Em todo o país, entre cinco e dez mil indivíduos são atingidos anualmente, dos quais cerca de 10% não sobrevivem. Certamente, a mortalidade não seria tão alta se a doença fosse diagnosticada e tratada mais precocemente. No entanto, de acordo com Sabroza, além de seu início lento e mal definido (o que dificulta o diagnóstico), os serviços de saúde ainda não se encontram suficientemente mobilizados para enfrentá-la, havendo, portanto, escassez de informação sobre a moléstia. Dois aspectos do processo de transmissão apresentam características que contribuem para a disseminação da leishmaniose visceral. O primeiro é o seu principal reservatório - o cão -, o segundo é o inseto responsável por 99% das infecções: a Lutzomyia longipalpis, ambos com hábitos urbanos. O cão é um animal essencialmente doméstico, completamente adaptado à vida junto ao homem e que inclusive se desloca com ele nas migrações. A L. longipalpis também já adequou sua sobrevivência ao que pesquisadores denominam de peridomicílio (as regiões ao redor das casas, como jardins, parques, bosques, hortas ou quintais). Além disso, até agora, não há vacina de eficácia comprovada e nem cura para a leishmaniose canina, de modo que a única alternativa é a eliminação do animal infectado - tanto como medida de controle da moléstia, quanto para evitar o seu sofrimento. No entanto, a população nem sempre se dispõe a eliminar seus bichos de estimação, o que mais uma vez ressalta a necessidade de um amplo trabalho de conscientização. Esporadicamente, os gatos também servem de reservatório para o protozoário. Em virtude do desmatamento, da migração de populações e das mudanças sociais e ambientais ocorridas nas últimas décadas, a leishmaniose visceral, antes silvestre, tornou-se uma doença urbana - apesar de ainda existir em focos rurais. Chega a uma cidade, segue a malha rodoviária, infectando as populações de beira de estrada, até atingir a periferia da próxima cidade. Diferentemente das tegumentares, a visceral pode inclusive atingir bairros bem urbanizados e centrais. Para sanar tal situação, urge que o problema da leishmaniose visceral seja encarado como de alta prioridade. Sabroza recomenda a completa integração entre profissionais de saúde do sistema privado e público, o envolvimento dos meios de comunicação em um movimento de conscientização, em conjunto com campanhas de esclarecimento e a conseqüente colaboração da população. A constituição de uma inteligência epidemiológica em locais endêmicos, diagnóstico e tratamento precoce e o diagnóstico e eliminação de cães infectados são outras medidas necessárias. Por fim, o controle da moléstia passa também por um controle vetorial, tema de trato extremamente complexo, exigindo a presença de profissionais especializados no assunto.
