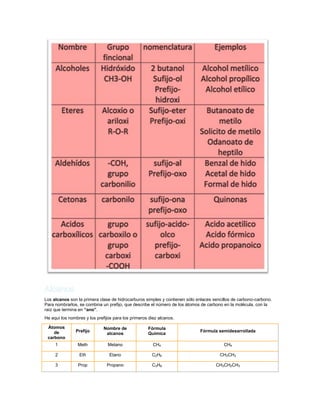
Alcanos
- 1. Los alcanos son la primera clase de hidrocarburos simples y contienen sólo enlaces sencillos de carbono-carbono. Para nombrarlos, se combina un prefijo, que describe el número de los átomos de carbono en la molécula, con la raíz que termina en “ano”. He aquí los nombres y los prefijos para los primeros diez alcanos. Átomos Nombre de Fórmula de Prefijo Fórmula semidesarrollada alcanos Química carbono 1 Meth Metano CH4 CH4 2 Eth Etano C2H6 CH3CH3 3 Prop Propano C3H8 CH3CH2CH3
- 2. 4 But Butano C4H10 CH3CH2CH2CH3 5 Pent Pentano C5H12 CH3CH2CH2CH2CH3 6 Hex Hexano C6H14 CH3CH2CH2CH2 CH2CH3 7 Hept Heptano C7H16 CH3CH2CH2CH2CH2CH2CH3 8 Oct Octano C8H18 CH3CH2CH2CH2CH2CH2CH2CH3 9 Non Nonano C9H20 CH3CH2CH2CH2CH2CH2CH2CH2CH3 10 Dec Decano C10H22 CH3CH2CH2CH2CH2CH2CH2CH2CH2CH3 La fórmula química para cualquier alcano se encuentra en la expresión CnH2n + 2, donde n es el número de carbonos que se enlazan. Ejemplo para un alcano que tenga seis carbonos (un hexano): CnH2n + 2 Reemplazamosn por el seis y tenemos C6H2(6) + 2 C6H12 + 2 C6H14 que según su fórmula semidesarrollada es CH3CH2CH2CH2CH2CH3 La fórmula semidesarrollada, para los primeros diez alcanos de la tabla, muestra cada átomo de carbono y los elementos a los que están unidos. Los alcanos simples comparten muchas propiedades en común. Todos entran en reacciones de combustión con el oxígeno para producir dióxido de carbono y agua de vapor. En otras palabras, muchos alcanos son inflamables. Esto los convierte en buenos combustibles. Por ejemplo, el metano es el componente principal del gas natural y el butano es un fluido común más liviano. Alquenos La segunda clase de hidrocarburos simples son los alquenos, formados por moléculas que contienen por lo menos un par de carbonos de enlace doble. Para nombrarlos, los alquenos siguen la misma convención que la usada por los alcanos. Un prefijo (para describir el número de átomos de carbono) se combina con la terminación “eno” para denominar un alqueno (no puede haber un meteno ya que tendría solo un átomo de carbono). El eteno (que sería el primer alqueno), por ejemplo, consiste de dos moléculas de Eteno, dos carbono unidas por un enlace doble. carbonos con enlace doble. La fórmula química para los alquenos simples sigue la expresión CnH2n. Debido a que uno de los pares de carbono está doblemente enlazado, los alquenos simples tienen dos átomos de hidrógeno menos que los alcanos. Alquinos Los alquinos son la tercera clase de hidrocarburos simples y son moléculas que contienen por lo menos un par de enlaces de carbono, que en este caso será triple. Tal como los alcanos y alquenos, los alquinos se denominan al combinar un prefijo (que indica el número de átomos de carbono) con la terminación “ino” para denotar un enlace triple. Etino, dos carbonos con enlace triple. La fórmula química para los alquinos simples sigue la expresión CnH2n-2. Isómeros
- 3. Ya que el carbono puede enlazarse de tantas diferentes maneras, una simple molécula puede tener diferentes configuraciones de enlace. Como ejemplo de tal afirmación, veamos las dos moléculas siguientes: CH3 CH3CH2CH2CH2CH2CH3 I CH3 CH2 CH CH2 CH3 C6H14 C6H14 Ambas moléculas tienen formulas químicas idénticas (C6H14), sin embargo sus fórmulas desarrolladas y estructurales (y, por consiguiente, algunas propiedades químicas) son diferentes. Estas dos moléculas son llamadas isómeros. Los isómeros son moléculas que tienen la misma fórmula química, pero diferentes fórmulas desarrolladas y estructurales. Clasificación de los compuestos orgánicos Como ya dijimos, los hidrocarburos, formados solo por carbono e hidrógeno, son los compuestos orgánicos más simples en su composición, por ello es que se pueden tomar como base para hacer una clasificación de los compuestos orgánicos. Si en un hidrocarburo sustituimos uno o más átomos de hidrógeno por otro átomo o agrupación de átomos podemos generar todos los tipos de compuestos orgánicos conocidos. Por ejemplo, si en un alcano (hidrocarburo saturado) sustituimos un átomo de hidrógeno por un halógeno obtendremos un derivado halogenado, y si en un alcano sustituimos dos átomos de hidrógeno por uno de oxígeno podemos general un aldehído (si la sustitución ocurre en un átomo de carbono terminal) o una cetona (si la sustitución se hace en un carbono intermedio). Entendido esto, podemos clasificar los compuestos orgánicos en hidrocarburos e hidrocarburos sustituidos. Si la sustitución de átomos de hidrógeno en los hidrocarburos se hace con átomos de oxígeno, hablaremos de compuestos oxigenados o funciones oxigenadas (alcoholes, fenoles, éteres, aldehídos, cetonas, ácidos, ésteres, sales).
- 4. Si la sustitución de átomos de hidrógeno en los hidrocarburos se hace con átomos de nitrógeno, hablaremos de compuestos nitrogenados o funciones nitrogenadas. ¿Qué es un grupo funcional? Hemos visto que los hidrógenos de los hidrocarburos pueden ser sustituidos por átomos de otro metal o por un agrupamiento de átomos para obtener compuestos derivados que poseen propiedades muy diferentes y que presentan estructuras muy distintas (el átomo o grupo de átomos sustituyentes les confieren otras propiedades físicas y químicas). Pues bien, a ese átomo o grupo de átomos que representan la diferencia entre un hidrocarburo y el nuevo compuesto, se le llama grupo funcional. Como corolario, podemos decir que un grupo funcional es un átomo o grupo de átomos que caracteriza a una clase de compuestos orgánicos. Cada grupo funcional determina las propiedades químicas de las sustancias que lo poseen; es decir determina su función química. Entonces, se llama función química a las propiedades comunes que caracterizan a un grupo de sustancias que tienen estructura semejante; es decir, que poseen un determinado grupo funcional. Por ejemplo, en un alcano, los átomos de hidrógeno pueden ser sustituidos por otros átomos (de oxígeno o nitrógeno, por ejemplo), siempre que se respete el número correcto de enlaces químicos (recordemos que el oxígeno forma dos enlaces con los otros átomos y el nitrógeno forma tres). El grupo OH en el alcohol etílico y el grupo NH2 en la etilamina son grupos funcionales. Reiteramos: La existencia de un grupo funcional cambia completamente las propiedades químicas (la función química) de la molécula. A título de ejemplo, el etano, alcano con Etanol dos carbonos, es un gas a temperatura ambiente; el etanol, el alcohol de dos carbonos (derivado del etano por sustitución), es un líquido. El etanol, el alcohol que se bebe comúnmente, es el ingrediente activo en las bebidas "alcohólicas" como la cerveza y el vino. Los principales grupos funcionales son los siguientes: Grupo hidroxilo (– OH) Es característico de los alcoholes, compuestos constituidos por la unión de dicho grupo a un hidrocarburo (enlace sencillo). Grupo alcoxi (R – O – R) Grupo funcional del tipo R-O-R', en donde R y R' son grupos que contienen átomos de carbono, estando el átomo de oxígeno en medio de ellos, característico de los éteres (enlace sencillo). (Se usa la R ya que estos grupos de átomos constituyen los llamados radicales) Grupo carbonilo (>C=O) Su presencia en una cadena hidrocarbonada (R) puede dar lugar a dos tipos diferentes de sustancias orgánicas: los aldehídos y las cetonas. En los aldehídos el grupo C=O está unido por un lado a un carbono terminal de una cadena hidrocarbonada (R) y por el otro, a un átomo de hidrógeno que ocupa una posición extrema en la cadena. (R–C=O–H) (enlace doble). En las cetonas, por el contrario, el grupo carbonilo se une a dos cadenas hidrocarbonadas, ocupando por tanto una situación intermedia. (R–C=O–R) (enlace doble). Ver: PSU: Química; Pregunta 05_2005(Química2) Es el grupo funcional característico de los ácidos orgánicos.
- 5. Los ácidos orgánicos reaccionan con los alcoholes de una forma semejante a como lo hacen los ácidos inorgánicos con las bases en las reacciones de neutralización. En este caso la reacción se denomina esterificación, y el producto análogo a la sal inorgánico recibe el nombre genérico de éster. Puede considerarse como un grupo derivado del amoníaco (NH3) y es el grupo funcional característico de una familia de compuestos orgánicos llamados aminas. Funciones oxigenadas A continuación, un cuadro resumen de los grupos funcionales (con su correspondiente función química) donde participan átomos de carbono, hidrógeno y oxígeno. Presencia de algún enlace carbono-oxígeno: sencillo (C-O) o doble (C=O) Función o Grupo funcional Fórmula Estructura Prefijo Sufijo compuesto Grupo hidroxilo Alcohol R-OH hidroxi- -ol Grupo alcoxi (o Éter R-O-R' -oxi- R-ilR'-iléter ariloxi) -al Aldehído R-C(=O)H oxo- -carbaldehído Grupo carbonilo R-C(=O)- Cetona oxo- -ona R' Grupo carboxilo Ácido carboxílico R-COOH carboxi- Ácido -ico - R-ato de R'- Grupo acilo Éster R-COO-R' iloxicarbonil- ilo Funciones nitrogenadas A continuación, un cuadro resumen de los grupos funcionales (con su correspondiente función) donde participan átomos de carbono, hidrógeno y nitrógeno. Presencia de enlaces carbono-nitrógeno, simples (C – N), dobles (C = N) o triples (C ≡ N) Grupo Función o Fórmula Estructura Prefijo Sufijo funcional compuesto
- 6. Amina R-NR2 amino- -amina Grupo amino Imina R-NCR2 _ _ R-C(=O)N(- Amida _ _ R')-R" Grupos amino y carbonilo Grupo nitro R-NO2 nitro- Nitrocompuesto Nitrilo o cianuro R-CN ciano- -nitrilo Isocianuro R-NC alquilisocianuro _ Grupo nitrilo Isocianato R-NCO alquilisocianato _ Grupo azo Azoderivado R-N=N-R' azo- -diazeno R1R2N- _ Hidrazina _ -hidrazina NR3R4 - _ Hidroxilamina -NOH _ hidroxilamina Funciones halogenadas A continuación, un cuadro resumen de los grupos funcionales donde participan átomos de carbono, hidrógeno y elementos halógenos. Compuestos por carbono, hidrógeno y halógenos. Fórmula del Tipo de compuesto Prefijo Sufijo Grupo funcional compuesto
- 7. Grupo haluro Haluro R-X halo- _ Grupo acilo Haluro de ácido R-COX Haloformil- Haluro de -oílo Alejandra Zuñiga Mendoza