Semana6.docxrtf
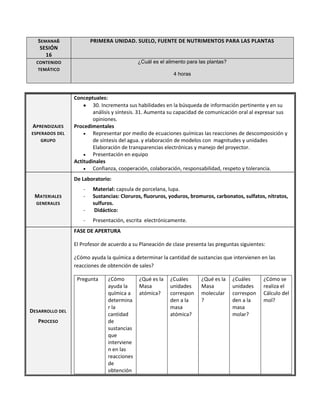
- 1. SEMANA6 SESIÓN 16 PRIMERA UNIDAD. SUELO, FUENTE DE NUTRIMENTOS PARA LAS PLANTAS CONTENIDO TEMÁTICO ¿Cuál es el alimento para las plantas? APRENDIZAJES ESPERADOS DEL GRUPO 4 horas Conceptuales: 30. Incrementa sus habilidades en la búsqueda de información pertinente y en su análisis y síntesis. 31. Aumenta su capacidad de comunicación oral al expresar sus opiniones. Procedimentales Representar por medio de ecuaciones químicas las reacciones de descomposición y de síntesis del agua. y elaboración de modelos con magnitudes y unidades Elaboración de transparencias electrónicas y manejo del proyector. Presentación en equipo Actitudinales Confianza, cooperación, colaboración, responsabilidad, respeto y tolerancia. De Laboratorio: - Material: capsula de porcelana, lupa. Sustancias: Cloruros, fluoruros, yoduros, bromuros, carbonatos, sulfatos, nitratos, sulfuros. Didáctico: - MATERIALES - Presentación, escrita electrónicamente. GENERALES FASE DE APERTURA El Profesor de acuerdo a su Planeación de clase presenta las preguntas siguientes: ¿Cómo ayuda la química a determinar la cantidad de sustancias que intervienen en las reacciones de obtención de sales? Pregunta DESARROLLO DEL PROCESO ¿Cómo ayuda la química a determina r la cantidad de sustancias que interviene n en las reacciones de obtención ¿Qué es la Masa atómica? ¿Cuáles unidades correspon den a la masa atómica? ¿Qué es la Masa molecular ? ¿Cuáles unidades correspon den a la masa molar? ¿Cómo se realiza el Cálculo del mol?
- 2. de sales? Equipo Respuesta 4 La química tiene varios tipos de unidades que ocupa para calcular las reacciones químicas y para calcular las sales por ejemplo el mol : La masa molecular relativa es un número que indica cuantas veces mayor es la masa de una molécula de una sustancia con respecto a la unidad de masa atómica. Su unidad es el Dalton o unidad de masa atómica que se abrevia(u). 2 La masa atómica del átomo de un elemento se refiere a la masa promedio de los átomos de un elemento. Se constituye por el número de protones más el número de electrones y se represent a con una “A” mayúscula . A= Masa atómica. A= N° de protones + el N° de neutrones . A= z+n 3 Está definida como la doceava parte (1/12) de la masa de un átomo neutro y no enlazado de carbon o-12, en su estado fundament al eléctrico y 3 nuclear, y su valor recomend ado es el de 1,660 538 921 (73) × −27 10 kg. Así pues, unmol de átomos de carbono12 tiene una masa exacta de 12 gramo s. Cuando decimos, por ejemplo, que el litio (Li) tiene una masa de 6,94 Da queremos decir que un átomo 5 La masa molecular es un número que indica cuantas veces mayor es la masa de una molécula de una sustancia respecto a la unidad de masa atómica. Su unidad es el Dalton o unidad de masa atómica que se abrevia “u” (antes uma) 1 Gramos sobre mol. grs/mol 6 Para calcular la masa molar se necesita saber: La masa atómica de cada uno de los elementos que constituye n la substancia . Lo primero es sacar el peso molecular de la sustancia, por ejemplo el peso molecular del agua (H2O) es de 18 g/mol, ya que el peso del Oxígeno es de 16g y el del Hidrógeno 1g, y en el agua hay 2 Hidrógeno s (2g) + 1 Oxígeno (16g) = 18g
- 3. de litio tiene la misma masa que 6,94 veces la masa de 1/12 parte de un átomo de carbono12. Por otro lado, la masa de 1 mol (NA) de unidades de masa atómica equivalen a 1 g. En el Sistema Internacio nal de Magnitude s (ISO 80000-1), se da como único nombre el de Dalton y desaconse ja el de unidad de masa atómica unificada, ya que esta tiene dos
- 4. valores. La unidad de masa atómica unificada no admite prefijos multiplicati vos, al contrario que el dalton; por lo que no es posible usar ku, pero sí kDa. Cada integrante del equipo lee diferente contenido sobre la misma pregunta. FASE DE DESARROLLO Procedimiento: � Investigación y discusión sobre los principales nutrimentos (macronutrimentos y micronutrimentos) para las plantas: - Forma química asimilable. - Necesidad de reposición en el suelo. (A30, A31) Masa molar Mol-Mol - Observar cada una de las sustancias con la lupa De acuerdo al número de lista cada alumno calculara el número de mol para cien gramos de la sustancia: Observaciones: A lo largo de la actividad se pudo observa la manera en la que los compañeros asimilaban el tema y como resolvían los cuestionamientos y el procedimiento
- 5. planteado, como algunos comprendías bien el tema y otros no tanto
- 7. No de lista Nombre de la sustancia Formula Masas atómicas Masa molecular Gramos/mol Numero de MOL para 100g de sustancia 1 Carbonato de sodio Na2CO3 Na:45.978 105.986 1.056 C:12.011 g/mol O:47.997 2 3 Sulfocianuro de Potasio KSCN K=39.102 90.1844 S=32.065 .901844 g/mol C=12.0107 N=14.0067 4 CLORURO DE POTASIO KCL 6 Carbón Activado. C 7 Cloruro de NH4Cl 5 124.555 G/MOL 0.802 C: 12.011 12.011 8.33 N: 14.006 53.4906 0.53491 K- 89.102 Cl- 35.453
- 8. amonio H:4.03116 35.453 Yoduro de Potasio KL 9 Nitrato de hierro Fe(NO3)3 10 Cloruro de Sodio NaCl Sulfato cúprico CuSO4 8 11 166.0064 g/mol 0.60238641mol Fe:56 N:28 O:96 241,86 g/mol 2.4186 Na= 28.9898 64.4428g/m ol 100/64.4428= 1.551763 MOL Cu 63.54 160.1776 .624307 S 32.64 Gr/mol K=39.102 L=126.9044 Cl=35.453 O(4) 63.9976 12 Nitrato de sodio NaNO3 Na:28.9898 N:14.0067 90.9965 gr/mol 1.098943366 O3:48.000 13 14 15 Cloruro Ferroso FeCl24H2O Fe:56 Cl:72 H:8 O:64 200g/mol 0.5 Mol 16 CLORURO DE POTASIO KCL K- 89.102 124.555 G/MOL 0.802 Yoduro de sodio NaI Na: 22.989 149.889 0.667 I:126.90 G/MOL Sulfato de Na2SO4 142.0412 142.04 17 18 Cl- 35.453 0.704021
- 9. Sodio 19 Nitrato de Sodio g/mol NaNO3 Sodio (1): 23 85 g/mol 1.17 Fe: 55.847 277.9044 0.359835 O11: 175.9934 g/mol g/mol 160.1776 GR/MOL .624307 MOL Na:22.98 149.88 1.499 I:126.9 Gr/mol mol K:39.098 165.998 grs/mol 0.602 mol 277.6325 gr/mol 0.3601883785 Mol Nitrogeno(1) : 14 Oxigeno (3): 48 20 Sulfato de hierro FeSO47H2O S:32.064 H: 14 21 Sulfato cuprico CuSO4 Cu- 63.54 S- 32.64 O4-63.9976 22 23 24 Yoduro de sodio NaI Yoduro de potasio Kl Nitrato de Cobre II Cu(NO3)2. 5H2O L:126.998 Cu- 63.0546 N2-28.0134 O11175.9934 H10-10.0797 25 Cloruro de calcio. CaCl2 75 110.986 g/mol 1.3333 mol 26 Nitrato de NaNO3 Na=23 85 g/mol 1.17 mol
- 10. Sodio N=14 O=48 27 28 29 30 Después discuten y sintetizan el contenido. Se preparan para mostrarlo a los demás equipos. Para simular las reacciones se les proporciona el nombre del programa cocrodile para que lo localicen en la Red y lo utilicen, es gratuito. FASE DE CIERRE Los equipos presentan su información a los demás. Al final de las presentaciones se lleva a cabo una discusión extensa, en la clase con el profesor, de lo que se aprendió. Actividad Extra clase: Los alumnos llevaran la información a su casa e indagaran los temas siguientes de acuerdo al cronograma. Elaboraran su informe, en un documento electrónico, para registrar los resultados en su Blog. EVALUACIÓN Producto: Presentación del. Resumen de la indagación bibliográfica. Actividad de Laboratorio. Indagación del programa gratuito simulador de reacciones químicas.