Thibault vha-vhe du2012
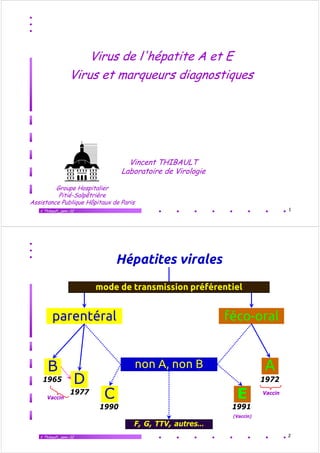
- 1. Virus de l'hépatite A et E p Virus et marqueurs diagnostiques Vincent THIBAULT Laboratoire de Virologie Groupe Hospitalier Pitié-Salpêtrière Assistance Publique Hôpitaux de Paris V.Thibault_janv.-12 1 Hépatites virales p mode de transmission préférentiel parentéral féco-oral féco oral B non A non B A, A 1965 D 1972 Vaccin 1977 C E Vaccin 1990 1991 (Vaccin) (V i ) F, G, TTV, autres… V.Thibault_janv.-12 2
- 2. V.Thibault_janv.-12 3 Historique VHA q Avant J.C.: “La Jaunisse” (Ikterus / kirrhos) 1745 : Cockayne, hépatites épidémiques y , p p q 1908 : McDonald, "notion de virus…" Reproduction de la maladie 1942 : p Volontaires (Voegt, Havens), Paul 1943 ingestion feces/serum Entité clinique : 1995 : Vaccin 17-18ème siècle - 1923 Blumer - 1947 McCallum (VHA "infectious"1996 : recommandations -VHB "serum") Transmission nosocomiale (préparation vaccinale : variole, fièvre jaune…) Visualisation : 1973 (Feinstone) 1999 : recommandations Développement de la sérologie : épidémiologie 1979 19 9 : culture (Provost et Hilleman) l (P H ll ) 1981... : Clonage, Séquences nucléotidiques 1991… Vaccination 1991 : V i ti 2006 : Déclaration obligatoire V.Thibault_janv.-12 4
- 3. Virus de l'hépatite A V.Thibault_janv.-12 5 Virus de l’Hépatite A • Famille : Picornaviridae Capside p (entérovirus type 72) • Genre : hépatovirus • Taille 27-32 nm 27-32nm • Non enveloppé ARN (+) • Structure icosaèdrique • ARN simple brin brin, Vpg • polarité positive • lié de façon covalente à une protéine Vpg V.Thibault_janv.-12 6
- 4. P1 prot. Capside P2 P3 0 Structurales Non structurales 7478 1B 1C 1D 2A 2B 2C 3 A-B 3C (PRO) 3D (POL) AAA Vpg 1A 2.5kDa IRES 3 Traduction 2A A-B (eIF-4G) (eIF 4G) poly- VP2 VP3 VP1 2B 2C 3C (PRO) 3D (POL) protéine VP4 2 227 AA ? Vpg Protéase Liaison NTP Hélicase ARN VP0 Polymérase VP2 VP3 VP1 Réplication Ré li ti VP4 2A VP2 VP3 VP1 X5 – X12 VP4 Protéines de surface 2A Maturation finale immunogénicité V.Thibault_janv.-12 7 Cycle de multiplication du VHA en culture de cellules Attachement Libération Réplication du génome Espace + de Disse - Traduction Synthèse + de la polyprotéine - P3 Maturation P2 Réticulum endoplasmique P1 Empaquetage Canalicule Relargage biliaire V.Thibault_janv.-12 8
- 5. Interférence du VHA avec les mécanismes de défense immunitaire Qu et al. PLoS Pathogens 2011 Vol. 7;9:e1002169 V.Thibault_janv.-12 9 Prédisposition génétique Hép. A / Allergie HAV-induced severe liver disease was associated with a 6-amino-acid insertion d h 6 d Meilleure liaison du VHA in TIM1/HAVCR1 (157insMTTTVP), the Forme + sévère gene encoding the HAV receptor. Kim et al. J Clin Invest. 2011;121(3):1111–1118. Chatenoud & Bach J Clin Invest. 2011; 121(3):848–850 V.Thibault_janv.-12 10
- 6. VHA : physiopathologie Absence d'effet cytopathique direct : d effet cytolyse résultant du processus immun de défense de l'hôte, médiation cellulaire édi ti ll l i médiation humorale V.Thibault_janv.-12 11 Propriétés Physiques du VHA p y q Agents Stabilité Chaleur Autoclavage (121°C, 20') Inactivation 100°C Inactivation 60°C Stable heure St bl 1 h température ambiante Stable 1 mois (selles, eaux, sols) Plusieurs jours sur surface sèche 4 h Sur les mains h. S l i 4°C Stable plusieurs mois Congelé Stable des mois ou années Acide-base A id b pH 1 : stable 5 h H t bl h. PH 3-11 : stable au moins 30' U.V. Inactivation Chimiques Chlore, ozone, Inactivation glutaraldéhyde, iode Alcool 70° 3' : inactivation partielle V.Thibault_janv.-12 12
- 7. VHA et agents physiques ou chimiques http://www.invs.sante.fr/publications/2009/guide_hepatite_a V.Thibault_janv.-12 13 Variabilité génétique P1 prot Capside prot. P2 P3 0 Structurales Non structurales 7478 1B 1C 1D 2A 2B 2C 3 A-B 3C (PRO) 3D (POL) AAA Vpg 1A 2.5kDa Comparaison nucléotidique C i lé tidi 6 Génotypes : IA,B ; II; IIIA,B ; IV-VI ⌦Homme : génotype I (90%), (III, II) ⌦Singes : IV, V, VI Sérotype unique é ⌦Nombre limité d'épitopes antigéniques VP1, VP3 ⌦Tests immunologiques T i l i ⌦Vaccination (HM175, CR326) virus i i inactivé cultivé sur MRC 5 ti é lti é MRC-5 V.Thibault_janv.-12 14
- 8. Répartition mondiale des génotypes Génotypes infectant l'homme en noir , les singes en rouge. Souche PA21 (génotype IIIA), isolée d'un singe Panamanian Owl en vert. (g yp ), g Cristina J, Costa-Mattioli M. Virus Res. 2007 Aug;127(2):151-7. V.Thibault_janv.-12 15 Phylogénie et facteurs de risque n=1156 cases Klevens et al. Arch Intern Med. 2010;170(20):1811-1818 V.Thibault_janv.-12 16
- 9. Epidemiology and Genetic Characterization of Hepatitis A Virus Genotype IIA Vi us G n t p IA IB Diffusion du génotype IIA en IIB France à partir d'une origine p g Autochtones A h Africaine IIA West Africa VP1 sequences (900 nt.) IIIB Desbois et al. J CLIN MICROBIOLOGY, IIIA 2010, 48, 9:3306–3315 V.Thibault_janv.-12 17 Génotypes et sévérité de l'hépatite Globalement, pas de consensus pour un lien direct entre le génotype et la sévérité de l'atteinte hépatique – Données en faveur de facteurs liés à l'hôte (TIM-HAVCR). Hepatitis A Virus Genotype and Its Correlation With the Clinical Outcome of Acute Hepatitis A in Korea: 2006–2008 p Yun et al. J. Med. Virol. 83:2073–2081 (2011) •n=556 (497 ARN positifs) Sept. 2006 à Août 2008 •Génotype IIIA induit des symptômes plus sévères yp y p p Comparative Analysis of Disease Severity Between Genotypes IA and IIIA of H d f Hepatitis A Vi titi Virus Yoon et al. J. Med. Virol. 83:1308–1314 (2011) •n=111, comparaison de deux périodes 1998 et 1999 (IA) (n = 45) et 2009 (IIIA) ( = 66) (n •IIIA plus sévère (ALAT et durée hospitalisation) V.Thibault_janv.-12 18
- 10. VHA : Paramètres Biologiques Ac anti-VHA = hépatite A ancienne ou vaccination IgM anti-VHA = hépatite aiguë A (clinique) protection contre réinfection Ag foie IgG Symptomes Ictère VHA Selles IgM VHA Sang 0 1 2 3 4 5 6 7 8 9 10 24 Semaines 19 V.Thibault_janv.-12 IgM HAV uniquement à bon escient ! 1% 11 % 82 % Faux positifs = 30% p Roque Afonso et al. CID 2006:42 -887 Alaska : test "réflexe" si Ig-VHA totales + réflexe Ig VHA Ig M HAV ⌦32 % de faux + (Castrodale CID 2005:41;e86) Vaccination : 8 à 20 % d'IgM VHA + dans les 2 à 3 semaines suivant l'injection… NE RECHERCHER L'IgM anti-VHA QU'EN CAS D'HEPATITE AIGUË V.Thibault_janv.-12 20
- 11. Marqueurs biochimiques Diagnostic ⌦ Transaminases (ALAT, ASAT) ⌦ Bili bi Bilirubine ⌦ Phosphatase alcaline ⌦ Facteurs de coagulation F g Sérologie +++ IgM anti VHA : infection récente IgG anti VHA : infection passée ou vaccination IgM et IgG anti VHA ti direct ( ) [ i Diagnostic di Di t (-) [uniquement d t dans l cadre d'ét d ] le d d'études] Virémie : techniques sensibles (105 v./mL) Recherche de virus dans les selles, prolongée, importante (109v./mL), épidémiologie Salive S li : IgG (ELISA) V.Thibault_janv.-12 Génome viral (RT-PCR) 21 Quantification de la virémie ? Limite de quantification 11 Hépatites A Normann et al., Journal of Medical Virology 72:10–16 (2004) 72:10 16 Hépatite fulminante Evolution bénigne Fujiwara K et al. 50 Hépatites A dont 19 fulminantes (10 OLT) p f ( ) J. Med Virol. 2011 Feb;83(2):201-7. Hépatite fulminante : Hepatitis A viral load in relation to -virémie (p=0.03) * severity of the infection. -bilirubine -(p=0.04) * 11 patients with fulminant hepatitis -age (p=0 09) age (p=0.09) 10 with severe acute hepatitis -génotype non IA (p=0.09) 70 with self-limited acute hepatitis Rezende et al., Hepatology 38:613-618 (2003) V.Thibault_janv.-12 22
- 12. Durée de la virémie: conséquences cliniques et biologiques 6-7 5-6 2-5 Log particules/mL Suivi de 13 patients : durée moyenne 95 jours Suivi de 27 patients dont 2 avec rechute (1-2 mois) High and Persistent Excretion of Hepatitis A Duration of viremia in hepatitis A virus p Virus in Immunocompetent Patients infection Tjon et al. Bower et al. Journal of Infectious Diseases Journal of Medical Virology 78:1398–1405 (2006) 2000;182:12–7 V.Thibault_janv.-12 23 Hépatite A : le vaccin virus inactivé AVAXIM 160U suspension injectable seringue préremplie ⌦ Virus de l'hépatite A souche GBM cultivée sur cellules diploïdes humaines MRC- p p 5 , inactivé HAVRIX 1 440 U Elisa/ml susp inj IM Ad en seringue HAVRIX 720 U Elisa/0,5 ml susp inj IM Enf/Nour en seringue El / l E f/ ⌦ Souche HM 175 du virus de l'hépatite A cultivée sur cellules humaines diploïdes MRC5 p Le schéma vaccinal habituel comprend 1 dose suivie d'un rappel (1 dose) 6 à 12 mois plus t d i l tard. La persistance des anticorps anti-VHA après vaccination n'est actuellement pas connue . Les données disponibles suggèrent la persistance des anticorps anti-VHA à un niveau protecteur au moins jusqu'à 20 ans après primo-immunisation. Hepatitis A Vaccine versus Immune Globulin for Post-exposure Prophylaxis Victor et al. 2007 N Engl J Med 357;17 V.Thibault_janv.-12 24
- 13. Difficultés diagnostiques En routine Adresser prélèvements au Centre national de référence du VHA Laboratoire de virologie Hôpital Paul Brousse 12-14 P l V ill t Couturier 12 14 av Paul Vaillant C t i 94804 Villejuif cedex Tel : 01 45 59 37 21 http://invs.sante.fr/surveillance/cnr/liste V.Thibault_janv.-12 25 SRAS ? Hépatite E ? Grippe V.Thibault_janv.-12 26
- 14. Historique VHE Découverte dépendante de la connaissance des virus des hépatites ⌦1955 : Inde, hépatite chez des personnes immunisées contre le VHA, épidémie VHA é idémi particulière. "NANBH" ti liè Entité clinique 1980 - similitude avec l’hépatite A : Inde : prévalence de l hépatite A importante l’hépatite Epidémie : autre virus des hépatites, contamination par l’eau 1983 : reproduction de l’hépatite non A-non B chez un volontaire p p immunisé contre VHA (Balayan) Hépatite à J36 J28-45, visualisation de particules virales > VHA (27-30nm) Reproduction de l’infection chez le singe (cynomolgus) Hépatite "non A - non B à transmission entérique (ENANB) non B" 1990 : Reyes et al. clonage et séquençage "VHE" 1991 : Tam et al. VHE 2000 : Panda et al. cDNA infectieux V.Thibault_janv.-12 27 Coloured transmission electron micrograph of hepatitis E virus particles (purple) Holmberg, Lancet Vol 376 September 11, 2010 V.Thibault_janv.-12 28
- 15. VHE Virus non enveloppé Sphérique (SRV) Famille : Hepeviridae Surface irrégulière Genre : Hepevirus Capside 27-34 nm 27 34 Symétrie icosaédrique ARN simple brin hélice droite polarité + 7,5kb poly-A poly A extrémité 3’ 3 Stabilité Au laboratoire : instable(-70 à +8°C) Décongélation/congélation Tractus GI : stable (pH) V.Thibault_janv.-12 29 Organisation génomique Non t N structurales t l Structurales St t l 7 200 nt ARN polarité + p 3’NC 5’ NC 28 5109 7124 Poly-A 5109 ORF3 114 AA MeT Y Pro P X Hel RdRp 5123 ORF2 660 AA G notyp s Génotypes 1-4 Protéines P téi DIAGNOSTIC immunogènes Hétérogénéité génétique Au moins 4 groupes majeurs (<20% hétérogénéité ORF2) subdivisés en 24 sous groupes dont homologues animaux Epitopes majeurs : parties C t d l’ORF3 et ORF2 E it j ti C-ter de t Protection croisée entre différentes souches : un seul sérotype ⌦ Développement de tests sérologiques (performances équivalentes entre les différents types ?) ffé ⌦ Vaccin : ORF 2 recombinante V.Thibault_janv.-12 30
- 16. Répartition des différents génotypes Aggarwal Hepatology 2011 V.Thibault_janv.-12 31 Similarités des souches humaines et animales Bilic et al. Journal of General Virology (2009), 90, 863–873 Sporadique Epidémique humaines aviaires Unrooted phylogenetic tree of four avian HEV and nine mammalian HEV isolates, based on the complete genome region V.Thibault_janv.-12 32
- 17. Etudes des souches de l'homme (n=100) et du porc (n=43) en France p ( ) Bouquet et al. Emerging Infectious Diseases Vol. 17, No. 11, November 2011 V.Thibault_janv.-12 33 Homologie des souches de l'homme et du porc p Bouquet et al. Emerging Infectious Diseases Vol. 17, No. 11, November 2011 V.Thibault_janv.-12 34
- 18. VHE du lapin… Cossaboom et al. Emerging Infectious Diseases Vol. 17,11, Nov 2011 V.Thibault_janv.-12 35 V.Thibault_janv.-12 36
- 19. Culture et Modèles animaux • Culture Difficile Culture primaire d’hépatocytes de macaques (cynomolgus) Cellules PLC/PRF/5 hépatocarcinome et "A549" cellules cancer A549 poumon (Tanaka et al. J. Gen Virol. 2007; Takahashi et al. Arch. Virol. 2012) Cellule embryonnaire • Modèles animaux Primates : reproduction de la pathologie humaine Volontaires... VHE du porc, du poulet Présence d’Ac chez poulet, porc, rat, souris, mouton... Lapin… Ma H et al. Experimental infection of rabbits with rabbit and genotypes 1 and 4 hepatitis E viruses. PLoS One. 2010 Feb 11;5(2):e9160 V.Thibault_janv.-12 37 Résistance thermique du VHE… VHE dans des suspensions fécales : Inactivation : 70°C 10' ou 95°C 1 min; I ti ti i 56 °C 30 min maintien de l'infectiosité Tanaka et al. J. Gen Virol. 2007 Colson et al. JID 2010:202 V.Thibault_janv.-12 38
- 20. VHE et contamination des eaux Presence of hepatitis A virus ( p (HAV) and hepatitis E virus ( ) p (HEV) in ) urban wastewater Prédominance du génotype 3 g yp J. Rodriguez-Manzano et al. Excretion patterns of HAV and HEV infections in Eastern Spain Journal of Water and Health 08.2 2010 V.Thibault_janv.-12 39 VHE : Paramètres Biologiques Khuroo MS, Khuroo MS. Seroepidemiology of a second epidemic of hepatitis E in a population that had recorded first epidemic Titre peu élevé p 30 years b f before and h d has b been under surveillance d ill protection contre réinfection ? since then. Hepatol Int. 2010 Feb 3;4(2):494-9 IgG Symptomes Ictère VHE Selles IgM VHE Sang 0 10 20 30 40 50 60 70 80 90 100 200 Jours 40 V.Thibault_janv.-12
- 21. Virémie et excrétion fécale Virémie Selles Détection du RNA-VHE chez 20 patients ayant une hépatite E aiguë Aggarwal et al. THE LANCET • Vol 356 • September 23, 2000, p1081-1082 Chandra NS et al. Dynamics of HEV viremia, fecal shedding and its relationship with transaminases and antibody response in patients with sporadic acute hepatitis E. V.Thibault_janv.-12 Virol J. 2010 Sep 6;7:213 41 Stratégie Diagnostique Pratique Hépatite aigue sans immunosuppression 1. IgM anti-VHE Délai d'obtention du résultat rapide 2. Recherche du génome du VHE (S 2 R h h d é d (Sang et Selles) t S ll ) Fiabilité des tests ? Hépatite dans un contexte d'immunosuppression d immunosuppression 1. Recherche du génome du VHE (Sang et Selles) 2. 2 Eventuellement quantification ARN VHE avant traitement ARN-VHE 3. Marqueurs sérologiques sans intérêt clinique Recherche d'anticorps (IgG) anti-VHE d anticorps Intérêt ? Fiabilité des tests ? V.Thibault_janv.-12 42
- 22. Stratégie Diagnostique g g q Se donner les moyens de faire le diagnostic Diagnostic Indirect Diagnostic Direct Recherche de l'immunité antivirale Recherche du génome sur IgM anti VHE prélèvements sang et selles IgG anti VHE Diagnostic Di ti IgG I G IgM RT-PCR I M RT PCR Certain +/- ++ + Probable +/- - + Douteux +++ - - Immunité + - - ancienne Huang S et al. 2010 Profile of Acute Infectious Markers in Sporadic Hepatitis E. PLoS ONE 5(10): e13560 V.Thibault_janv.-12 43 Stratégie Diagnostique (à adapter en fonction du lieu géographique...) p g g p q Marqueurs non biologiques circonstances de la maladie (voyage, autres causes, épidémie) A adapter en fonction de la zone géographique ? (Sud versus Nord ?) Priorité hépatite P i ité hép tit A ou hép tit E u hépatite Enquête alimentaire "profil" du patient (âge, facteurs de risque…) clinique : hépatite “classique”, absence de chronicité (chez l'immunocompétent ! ) Portage prolongé en cas d'immunodépression P l é d' dé Absence de marqueurs biologiques : diagnostic d'exclusion Absence des marqueurs des virus des autres hépatites (A, B, C, D) é Notions sérologiques pour d’autres virus (EBV, CMV, herpès) V.Thibault_janv.-12 44
- 23. Performance des tests sérologiques Panels 50 sérums ARN HEV (+), G3 406 sérums IgG ARN HEV (-) ( ) IgM anti-HEV Microplaque p q Microplaque p q Test rapide p Adaltis MP Diagnostics MP Diagnostics anti-HEV IgG positif négatif positif négatif positif négatif Positif (n=41) 40 1 39 2 37 4 Negatif (n=9) 5 4 5 4 4 5 Total (n=50) 45 5 44 6 41 9 Sensibilité 90 88 82 Spécificité p f 100 99.5 100 VPP 100 95.7 100 VPN 98.8 98.5 97.8 Legrand-Abravanel CLINICAL AND VACCINE IMMUNOLOGY, May 2009, p. 772–774 V.Thibault_janv.-12 45 Des données à affiner... % d'enfants ou de donneurs de sang positifs pour les IgG anti-VHE (test Wantai) Séroprévalence de 16.6% rapportée antérieurement... Séroprévalence par tranche d'âge é é l h d'â 80 70 70 62.1 Facteurs de risque : 60 56 âge 50 résidence rurale é id l 42.5 40 chasse % 32.8 contact avec les 30 chats 20 44% (n 18) de (n=18) 10 saucisses ARN-VHE + 3.7 0 24 2‐4 18 27 18‐27 28 37 28‐37 38 47 38‐47 48 57 48‐57 58 65 58‐65 n=188 n=64 n=106 n=184 n=116 n=40 Mansuy et al. 2011 Em. Inf. Dis 17;12,2309 46 V.Thibault_janv.-12
- 24. Performance des tests : détection du génome viral (RT-PCR) Panel de 24 échantillons envoyés à % de détection positive différents laboratoire 100 90 80 70 60 50 40 30 20 10 0 titre (log) 6.2 /5.2/4.2/3.2/2.2/1.2 6.4 /5.4/4.4/3.4/2.4/1.4 5.1 /4.1/3.1/2.1/1.1 5 /4 /3 /2 /1 HRC‐HE104 (3a) JRC‐HE3 (3b) RKI (3f) HRC‐HE15 (4c) Baylis et al. J. Clin. Microbiol. 2011, 49(4):1234. V.Thibault_janv.-12 47 HEV – virémie- selle transmission ran m n serum salive Concentré de plaquettes à J0 Transfusé à un homme de 64 ans traité pour Lymphome non-Hodgkinien par GM IgG autologue IgM Matsubayashi K, et al. Transfusion. 2008 Jul;48(7):1368-75. V.Thibault_janv.-12 48
- 25. Immunodépression, hépatite chronique et stratégie diagnostique Dans le cadre d'une investigation chez un patient immuno déprimé, D l d d' i ti ti h ti t i dé i é La détection du génome viral (RT-PCR) sera privilégiée ! (ceci s'applique pour de nombreux diagnostics viraux - PCR) s applique Kamar et al. American Journal of Transplantation 2008; 8: 1744–1748 V.Thibault_janv.-12 49 VHE et vaccination 20 μg d'antigène rHEV (capside exprimée dans baculovirus) dans 0.5 ml de PBS sur 0.5 0 5 mg d'hydroxyde d'aluminium. d'h d d d' l i i 3 injections Moyenne géométrique du taux d'anticorps anti-VHE Efficacité : 95,5% après 3 doses Risque cumulé d'un premier épisode d'hépatite E Shrestha,et al 2007 N Engl J Med 356;9 V.Thibault_janv.-12 50
- 26. HEV 239 (Hecolin; Xiamen Innovax Biotech, Xiamen, China), produced in bacterial cells : VHE et vaccination safe and efficacious against infection with hepatitis E virus in seronegative participants in a phase 2 trial Zhu et al Lancet. 2010 Sep 11;376(9744):895-902 V.Thibault_janv.-12 51 Difficultés diagnostiques En routine Adresser les prélèvements au Centre national de référence du VHA/VHE Laboratoire de virologie Hôpital Paul Brousse 12-14 P l V ill t Couturier 12 14 av Paul Vaillant C t i 94804 Villejuif cedex Tel : 01 45 59 37 21 http://invs.sante.fr/surveillance/cnr/liste V.Thibault_janv.-12 52