Química General I - Estados de la materia, ley de los gases y teoría cinético-molecular
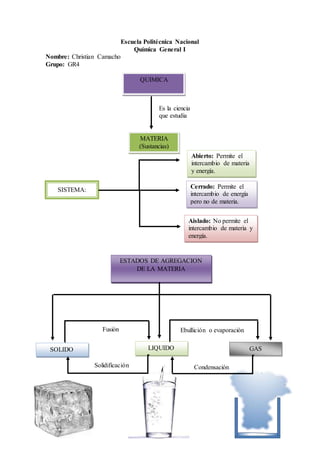
- 1. Escuela Politécnica Nacional Química General I Nombre: Christian Camacho Grupo: GR4 QUIMICA MATERIA (Sustancias) Abierto: Permite el intercambio de materia y energía. SISTEMA: Cerrado: Permite el intercambio de energía pero no de materia. Aislado: No permite el intercambio de materia y energía. Es la ciencia que estudia ESTADOS DE AGREGACION DE LA MATERIA SOLIDO LIQUIDO GAS Fusión Ebullición o evaporación Solidificación Condensación
- 2. VARIABLES DE ESTADO Son propiedades de un sistema que se pueden medir. PRESION: P=F/A TEMPERATURAMASA Medida de cantidad de materia (kg, g, TM, lbm,…) Presión Barométrica: Presión de un sitio o lugar. Temperatura de ebullición, normal H2O: 212ºF=100ºC=373K. Temperatura de fusión del hielo: 32ºF=0ºC=273K. Equivalencias: 1kg=1000g=10−3 TM=2.2lmb … Presión Manométrica: Presión de un recipiente cerrado medido con un manómetro Presión absoluta (P. abs.): P. abs. =P. bar. + P. man. Unidades: 1atm=760mmHg=76cmHg=10.31mH2O=14.69psi… LEY DE LOS GASES Escriba aquí la ecuación. Ecuación de estado: PV=nRT P=Presión V=Volumen n= número de moles R=constante de los gases ideales (0.082 L.atm/mol.K) T=Temperatura Peso o masa molecular (MM)= m/n Densidad (d)=m/V Fracción Molar 𝑦 𝐴= 𝑛 𝐴 𝑛 𝑇 = 𝑃 𝐴 𝑃 𝑇 = 𝑉 𝐴 𝑉𝑇Masa molecular de una mezcla de gases: 𝑀𝑀 𝑚𝑒𝑧𝑐𝑙𝑎 = 𝑦𝐴 𝑀𝑀𝐴 + 𝑦𝐵 𝑀𝑀 𝐵 + 𝑦𝑐 𝑀𝑀𝐶+…..
- 3. Estado sólido Estado líquido Estado gaseoso Predominan las fuerzas de cohesión sobre las de repulsión. Las partículas sólo pueden vibrar alrededor de su posición de equilibrio. Las fuerzas de cohesión y de repulsión son del mismo orden. Las partículas pueden desplazarse con cierta libertad pero sin alejarse unas de otras. Por esa razón los líquidos tienen volumen constante y se adaptan a la forma del recipiente. Predominan las fuerzas de repulsión sobre las de cohesión. Las partículas se mueven con total libertad y están muy alejadas unas de otras. Por eso los gases tienen forma variable y tienden a ocupar todo el volumen disponible. TEORIA CINETICA-MOLECULAR Para explicar el comportamiento de la materia y las características de los gases, los científicos propusieron, durante el siglo XIX, la denominada "teoría cinética de los gases". Su ampliación a líquidos y sólidos dio lugar al modelo cinético-molecular de la materia. Este modelo se basa en dos postulados fundamentales. La materia es discontinua, es decir, está formada por un gran nº de partículas separadas entre sí. Estas partículas materiales se encuentran en constante movimiento debido a dos clases de fuerzas: de cohesión y de repulsión Las fuerzas de cohesión tienden a mantener las partículas materiales unidas entre sí. Las fuerzas de repulsión tienden a dispersar las partículas y a alejarlas unas de otras. Según que predominen unas u otras fuerzas, la materia se presenta en estado sólido, líquido o gaseoso. REACCION EN FASE GASEOSA SUSTITUCION: 𝐴 + 𝐵𝐶 → 𝐵 + 𝐴𝐶 DESCOMPOSICION: 𝐴𝐵 → 𝐴 + 𝐵 FORMACION: 𝐴 + 𝐵 → 𝐴𝐵 DOBLE SUSTITUCION: 𝐴𝐵 + 𝐶𝐷 → 𝐷𝐵 + 𝐴𝐶 Reacción Química: 𝑎𝐴(𝑔) + 𝑏𝐵( 𝑔) → 𝑐𝐶(𝑔) + 𝑑𝐷(𝑔)
